Samenvatting
Dit rapport presenteert de resultaten van een uitgebreide analyse van de nauwkeurigheid van het Skinive AI-algoritme bij de analyse van huidbeelden van 2021 tot 2026. Tegenwoordig wordt kunstmatige intelligentie veel gebruikt in de dermatologie voor huidanalyse, het opsporen van huidaandoeningen en het identificeren van klinisch relevante veranderingen op foto’s die met mobiele apparaten zijn gemaakt.
Het algoritme werd geëvalueerd met behulp van een vaste validatiedataset van 27.829 huidbeelden, waardoor consistente en betrouwbare metingen van prestatieverbeteringen over verschillende fasen van de modelontwikkeling mogelijk waren. Oplossingen zoals Skinive worden steeds vaker gebruikt als digitale huidscreeningtools, waaronder moedervlekcontroles en AI-aangedreven huidscanners die huidaandoeningen op basis van beelden beoordelen.
Gedurende de studieperiode toonde het algoritme een gestage verbetering in de belangrijkste prestatiemetingen. Tegen 2026 bereikte de sensitiviteit 97,4%, de specificiteit 93,1% en de algehele nauwkeurigheid van huidbeeldanalyse 94,2%. De precisie nam toe tot 82,2%, wat wijst op een significante vermindering van fout-positieve resultaten bij het detecteren van huidaandoeningen.
De analyse van prestatieontwikkelingen toont een duidelijke verschuiving van een model dat voornamelijk gericht was op het detecteren van zoveel mogelijk afwijkingen, naar een meer gebalanceerd AI-systeem dat huidbeelden nauwkeurig kan analyseren en tegelijkertijd valse meldingen minimaliseert. Dit is bijzonder belangrijk voor mobiele huidscanner-apps en digitale dermatologietools, waarbij betrouwbaarheid direct invloed heeft op het vertrouwen van gebruikers en de klinische waarde.
Het algoritme is getraind met meer dan 3,5 miljoen huidbeelden, waarvan 250.000 beelden werden geselecteerd en gevalideerd door dermatologen om een klinisch betrouwbare trainingsdataset te creëren. Het gebruik van real-world gebruikersbeelden, gemaakt met smartphones, verbetert de robuustheid van het model voor variaties in belichting, hoek en beeldkwaliteit, wat resulteert in een nauwkeurigere AI-huidanalyse onder realistische omstandigheden.
Deze resultaten laten zien dat moderne AI-algoritmen huidbeelden met hoge nauwkeurigheid kunnen analyseren en tekenen van huidaandoeningen kunnen detecteren, terwijl een sterke balans tussen sensitiviteit en specificiteit behouden blijft. In de dermatologie worden dergelijke technologieën gebruikt voor beoordeling van huidgezondheid, analyse van moedervlekken, huidmonitoring en besluitvorming over het al dan niet raadplegen van een dermatoloog.
Waarom nauwkeurigheid belangrijk is bij AI-huidanalyse
In de afgelopen jaren is er steeds meer aandacht besteed aan hoe nauwkeurig kunstmatige intelligentie huidbeelden kan analyseren en klinisch relevante veranderingen kan detecteren. Dit is vooral belangrijk in het kader van vroege opsporing van hoogrisicocondities, waarbij tijdige evaluatie van huidveranderingen een cruciale rol kan spelen.
Huidziekten blijven een belangrijk wereldwijd gezondheidsprobleem. Volgens het Global Burden of Disease-onderzoek bedroeg de leeftijdgestandaardiseerde prevalentie van huidaandoeningen in 2021 1.017 gevallen per 100.000 mensen, met aanzienlijke regionale variatie [1].
Het spectrum van huidpathologie omvat meer dan 3.000 verschillende aandoeningen. Huidkanker is van bijzonder belang:
- Basaalcelcarcinoom is de meest gediagnosticeerde vorm van kanker wereldwijd.
- Melanoom, hoewel minder voorkomend, is verantwoordelijk voor het merendeel van de sterfgevallen door huidkanker [2].
In 2020 waren er wereldwijd 325.000 nieuwe melanoomgevallen, met overlevingspercentages variërend van 50% in Oost-Europa tot 80% in West-Europa, wat de verschillen in toegang tot screening, vroege diagnose en behandeling benadrukt [3].
Deze uitdaging wordt verder versterkt door het voortdurende tekort aan dermatologische specialisten. Volgens de Wereldgezondheidsorganisatie is het aantal dermatologen in veel Europese landen nog onvoldoende [4]. In dit kader worden AI-aangedreven huidanalysetools steeds belangrijker als schaalbare oplossingen voor screening en triage van patiënten [5].
Een groeiend aantal onderzoeken ondersteunt de effectiviteit van AI in de dermatologie. Een review uit 2025 van 551 studies toonde aan dat convolutionele neurale netwerken de hoogste diagnostische prestaties behalen, met 91% sensitiviteit en 94% specificiteit bij het onderscheiden van melanoom van goedaardige huidlaesies [6, 7].
Belangrijk is dat AI de diagnostische nauwkeurigheid aanzienlijk kan verbeteren bij huisartsen en niet-specialistische zorgverleners, met het grootste voordeel buiten de dermatologie [8].
Een meta-analyse uit 2024 die deep learning-algoritmen in de eerstelijnszorg evalueerde, rapporteerde sterke prestaties, met 90% sensitiviteit en 85% specificiteit bij het detecteren van verdachte gepigmenteerde laesies [9]. De diagnostische odds ratio bereikte 26,39 en de oppervlakte onder de ROC-curve was 0,95, wat duidt op uitstekende discriminerende capaciteit.
Deze resultaten zijn vergelijkbaar met die van ervaren dermatologen. Volgens een grote meta-analyse uit 2024 van 100 studies behaalden dermatologen die dermoscopie gebruikten 85,7% sensitiviteit en 81,3% specificiteit bij huidkankerdiagnose [10]. Opmerkelijk is dat ervaren dermatologen 13,3 keer meer kans hadden om een nauwkeurige diagnose te stellen dan huisartsen.
De COVID-19-pandemie versnelde de adoptie van teledermatologie. Enquêtes onder dermatologen toonden aan dat het gebruik van telemedicine steeg van 40% naar 90%, waarbij 87,5% een positievere houding rapporteerde ten opzichte van zorg op afstand [11].
De betrouwbaarheid van mobiele toepassingen met kunstmatige intelligentie voor het monitoren van het verloop van verschillende dermatologische aandoeningen, zoals atopische dermatitis, wordt ook bevestigd door wetenschappelijk onderzoek [12].
Vooruitgang in neurale netwerktechnologieën — waaronder continu hertrainen op representatieve datasets en verbeterde validatiestandaarden — heeft eerdere zorgen over de betrouwbaarheid van commerciële AI-oplossingen aangepakt [13].
Een voorbeeld is het Skinive AI-algoritme, dat consistente vooruitgang heeft laten zien bij de diagnose van een breed scala aan huidaandoeningen en is erkend door de wereldwijde wetenschappelijke gemeenschap [14, 15]. Deze vooruitgang weerspiegelt zich in de groeiende adoptie van de Skinive mobiele app, die tegen 2026 wereldwijd meer dan 1 miljoen downloads heeft bereikt. De geografische verdeling van Skinive-gebruikers wordt weergegeven in Figuur 1.
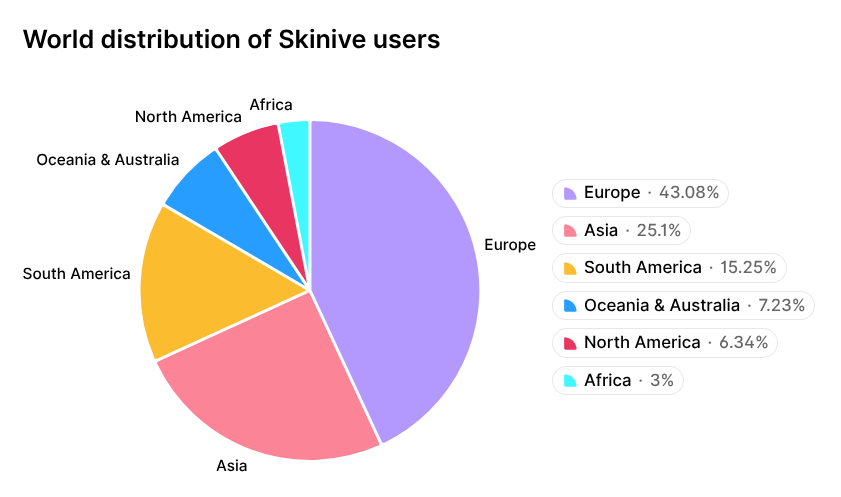
Figuur 1. Geografische verdeling van gebruikers van de Skinive mobiele app.
Tegen 2026 zijn AI-gestuurde oplossingen niet langer alleen ondersteunende hulpmiddelen—they zijn steeds meer geïntegreerd in de workflows van de gezondheidszorg, vooral gezien het aanhoudende tekort aan dermatologen en de groeiende behoefte aan vroege opsporing van kwaadaardige huidlaesies. Hierdoor is de nauwkeurigheid van AI-algoritmen in de dermatologie een cruciale factor geworden voor hun praktische toepassing. De vraag hoe betrouwbaar deze systemen tekenen van huidveranderingen kunnen detecteren, is zowel voor gebruikers als zorgprofessionals van centraal belang.
Ontwikkeling van het Skinive-algoritme voor huidbeeldanalyse
De vooruitgang van AI-algoritmen heeft directe invloed op de nauwkeurigheid van huidbeeldanalyse en de betrouwbaarheid bij het detecteren van huidziekten. In deze sectie wordt de ontwikkelingslijn van het Skinive-algoritme gepresenteerd, met nadruk op belangrijke verbeteringen in modelarchitectuur, datakwaliteit en beeldverwerkingssnelheid.
Het Skinive-neuraal netwerk is een multimodaal deep learning-systeem dat is ontworpen om de morfologische kenmerken van huidcondities te classificeren op basis van digitale afbeeldingen gemaakt met smartphonecamera’s. Door de jaren heen heeft het netwerk verschillende belangrijke verbeteringen ondergaan. De algoritmeverbeteringen richtten zich op het vergroten van de dataset, het optimaliseren van de modelarchitectuur en het verbeteren van de beeldverwerkingskwaliteit:
- 2020–2021 (Prototyping): Vroege versies waren gebaseerd op ResNet en vroege EfficientNet-architecturen. Het hoofddoel was het aantonen van een proof of concept (PoC) voor het analyseren van huidbeelden en het onderscheiden van goedaardige en potentieel schadelijke aandoeningen onder ongecontroleerde lichtomstandigheden.
- 2022–2023 (Validatie): De trainingsdataset groeide tot meer dan 160.000 geverifieerde afbeeldingen. Een Image Quality Module werd geïntroduceerd om lage kwaliteit of oninformatieve afbeeldingen te filteren.
- 2024 (Netwerkoptimalisatie): De architectuur van het neurale netwerk werd verfijnd door gerichte hyperparameteroptimalisatie.
- 2024–2026 (Opschaling en SOTA): Tegen 2026 adopteerde Skinive volledig geavanceerde deep learning-architecturen (Dino v3 Convnext), met een hoge inferentiesnelheid (360 ms per core). De uiteindelijke trainingsdataset werd uitgebreid tot 250.000 geannoteerde afbeeldingen, gelabeld door professionele dermatologen om hoogwaardige, klinisch gevalideerde data te garanderen. De introductie van de YOLO11-architectuur maakte real-time objectdetectie op huidbeelden via mobiele apparaten mogelijk en verbeterde de classificatienauwkeurigheid verder.
Deze voortdurende ontwikkelingen hebben de nauwkeurigheid van huidanalyse aanzienlijk verbeterd, de capaciteit van het algoritme om een breed scala aan huidcondities te detecteren vergroot en de impact van externe factoren zoals beeldkwaliteit of lichtomstandigheden verminderd.
Om aan de huidige klinische standaarden te voldoen, werd in 2026 de classificatie van herkende huidcondities geüpdatet en werden risiconiveaus verfijnd om de gezondheidsrelevantie en de noodzaak van consultatie bij een dermatoloog beter weer te geven.
Analyse van de verzamelde afbeeldingen, samen met feedback van gebruikers en partners, wees op de noodzaak om het neurale netwerk te trainen op aanvullende huidziekten en -condities. Hierdoor werd de lijst met herkenbare condities uitgebreid met urticaria, erythema, hidradenitis en vitiligo, naast het vermogen om gezonde nagels (zonder pathologie) te herkennen. De huidige classificatie van herkende huidcondities wordt weergegeven in Tabel 1.
Data en Trainingsdataset van Skinive voor AI-gebaseerde Huidanalyse
De kwaliteit en omvang van gegevens zijn cruciale factoren die de nauwkeurigheid van AI-algoritmen voor dermatologische analyse bepalen. Hoe diverser en klinisch gevalideerd de trainingsdataset, hoe beter het algoritme in staat is huidafbeeldingen correct te analyseren onder realistische omstandigheden.
In de loop van zes jaar nam het totale aantal door het neurale netwerk geanalyseerde afbeeldingen 300 keer toe, van 20.000 naar 6.000.000 afbeeldingen, waardoor de Skinive-dataset een van de grootste dynamisch bijgewerkte databases in de dermatologie wereldwijd is. De groeidynamiek wordt geïllustreerd in Figuur 2.
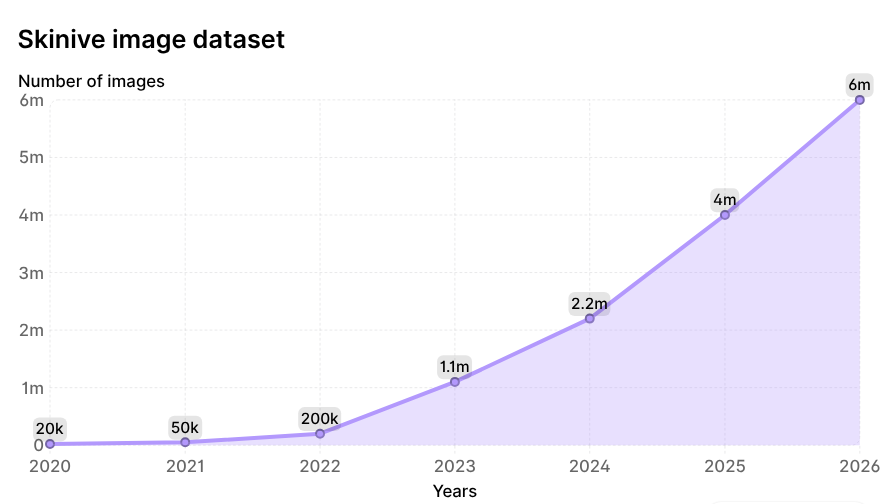
Figuur 2. Groeidynamiek van het aantal afbeeldingen geanalyseerd door het Skinive-neuraal netwerk sinds 2020.
De geografische verdeling van Skinive-gebruikers, met een overwegend Europees en Aziatisch aandeel, wordt vanzelfsprekend weerspiegeld in de samenstelling van huidfototypen volgens de Fitzpatrick-schaal in de wereldwijde dataset (Figuur 3). Deze verdeling zorgt voor een representatie van diverse huidfototypen en versterkt de robuustheid van het algoritme bij het analyseren van afbeeldingen van verschillende populaties.
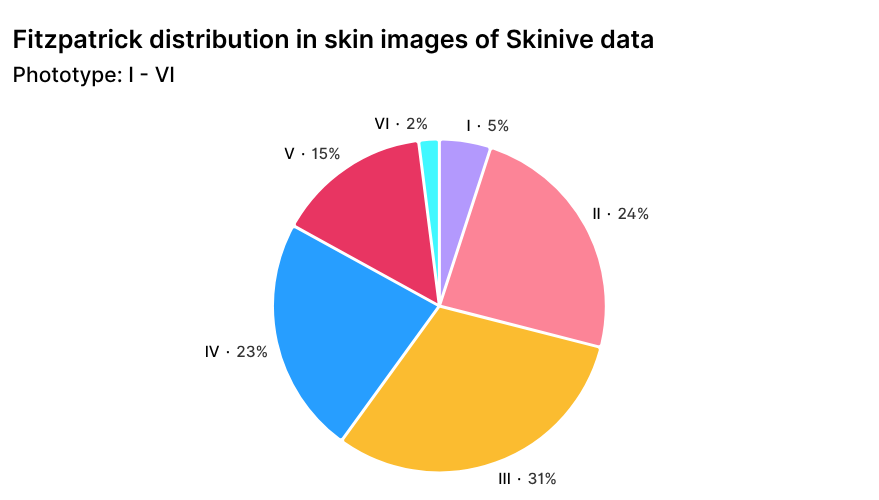
Figuur 3. Verdeling van Skinive-datasetafbeeldingen naar huidfototype volgens de Fitzpatrick-schaal.
Om de huidige trainingsdataset samen te stellen, analyseerde een deskundig panel van dermatologen 3,5 miljoen afbeeldingen. Als resultaat van een strikte klinische selectie bevatte de uiteindelijke trainingsdataset 250.000 referentieafbeeldingen van hoge kwaliteit (selectieratio ~7%). Dit zorgde voor een hoge mate van klinische validiteit en gegevensconsistentie (“Gold Standard”), wat cruciaal is voor het trainen van diepe neurale netwerken zoals Dino v3 Convnext en het mogelijk maakt om prestaties in de loop van de tijd objectief te beoordelen.
Voor de evaluatie van de nauwkeurigheid van het Skinive-algoritme werd een propriëtaire validatiedataset gebruikt, die in 2021 werd gecreëerd en gestandaardiseerd. Dit maakt een objectieve beoordeling van de prestaties van het algoritme in verschillende fasen van modelontwikkeling mogelijk. De validatiedataset bestond uit 27.829 afbeeldingen.
De combinatie van een grote dataset, klinische validatie en diversiteit in afbeeldingsomstandigheden vormt een sterke basis voor het verbeteren van de nauwkeurigheid van AI-gebaseerde huidanalyse en maakt het algoritme robuust tegen variabiliteit in afbeeldingen van echte gebruikers.
Methodologie voor het Evalueren van de Nauwkeurigheid van het Skinive-Algoritme
Het beoordelen van de nauwkeurigheid van AI-algoritmen is een cruciale stap in hun ontwikkeling en implementatie. Een rigoureuze evaluatiemethodologie maakt het mogelijk om vast te stellen hoe betrouwbaar het algoritme huidafbeeldingen analyseert en tekenen van dermatologische veranderingen detecteert onder diverse omstandigheden.
Dit rapport presenteert een interne, gestandaardiseerde longitudinale analyse van de nauwkeurigheid van het Skinive-algoritme van 2021 tot 2026. Het primaire doel was om de evolutie van de diagnostische prestaties van het model in de loop van de tijd te beoordelen tijdens iteratieve optimalisatie. In tegenstelling tot externe vergelijkende studies richt deze analyse zich niet op benchmarking tegen andere oplossingen, maar op het meten van de relatieve vooruitgang van het algoritme onder strikt gecontroleerde omstandigheden.
Om vergelijkbaarheid van resultaten over alle jaren te waarborgen, werd één enkele validatiedataset gebruikt, vastgesteld en gefixeerd in 2021. Deze dataset bestond uit 27.829 afbeeldingen die een breed scala aan dermatologische aandoeningen vertegenwoordigen, verzameld onder omstandigheden die nauw aansluiten bij het gebruik van mobiele apparaten in de praktijk. De validatiedataset bleef in de daaropvolgende jaren onveranderd en werd uitsluitend gebruikt om de prestaties van het model te evalueren, waardoor variabiliteit in de data als storende factor werd geëlimineerd en eerlijke vergelijkingen tussen verschillende versies van het algoritme mogelijk werden. Belangrijk is dat de validatiedataset na de creatie nooit voor training of retraining van het model werd gebruikt.
Het neurale netwerk werd getraind op een veel grotere dataset die was afgeleid van de verzamelde gebruikersafbeeldingen. Aanvankelijk werden meer dan 3,5 miljoen afbeeldingen geanalyseerd, waarvan 250.000 werden geselecteerd voor de uiteindelijke trainingsdataset. Selectie was gebaseerd op klinische relevantie en datakwaliteit. Alleen afbeeldingen die een eenduidige interpretatie van morfologische kenmerken mogelijk maakten en waarvan de annotaties waren geverifieerd, werden opgenomen. Afbeeldingen van lage kwaliteit of duplicaten, evenals gevallen met onzekere of ambiguë diagnoses, werden uitgesloten. Daarnaast werd rekening gehouden met klassebalans: wanneer de dataset een oververtegenwoordiging van veelvoorkomende goedaardige aandoeningen bevatte, kreeg zeldzamere en klinisch significante ziekten prioriteit.
Deze aanpak bij het samenstellen van de trainingsdataset zorgde voor een hoge gegevensintegriteit en minimaliseerde de invloed van ruis die onvermijdelijk aanwezig is in door gebruikers gegenereerde content. Tegelijkertijd behield de validatiedataset kenmerken van gebruik in de echte wereld, inclusief variabiliteit in verlichting, beeldkwaliteit en huidfototypes, waardoor de evaluatie zeer relevant is voor praktische toepassingen—met name voor huidafbeeldingen gemaakt met mobiele apparaten onder diverse omstandigheden.
Standaard classificatiemetrics werden gebruikt om het algoritme te evalueren, waaronder sensitiviteit, specificiteit, positieve voorspellende waarde (precisie), F1-score en algehele nauwkeurigheid. Alle metrics werden consistent berekend voor elke algoritmeversie met dezelfde validatiedataset, waardoor een objectieve beoordeling van veranderingen in prestaties in de loop van de tijd mogelijk was. Het gebruik van meerdere metrics biedt een uitgebreid beeld van de mogelijkheden van het algoritme, inclusief het vermogen om dermatologische aandoeningen te detecteren en tegelijkertijd valse positieven te minimaliseren.
Het moet worden opgemerkt dat deze analyse is gebaseerd op een intern validatiekader en bedoeld is om de evolutie van het algoritme binnen het Skinive-ecosysteem te evalueren. Het is geen externe klinische studie en biedt geen directe vergelijking met andere oplossingen of onafhankelijke datasets. Vergelijkende studies met externe klinische datasets zijn gepland als volgende stap in de ontwikkeling van het algoritme.
Resultaten: Nauwkeurigheid van Skinive AI Huidanalyse
In deze sectie worden de resultaten gepresenteerd van de evaluatie van de nauwkeurigheid van het Skinive-algoritme bij het analyseren van huidafbeeldingen. De focus ligt op kernmetrics zoals sensitiviteit, specificiteit en algehele nauwkeurigheid, die het vermogen van het algoritme weerspiegelen om dermatologische aandoeningen te detecteren en tegelijkertijd valse positieven te minimaliseren.
Analyse van het Skinive-neurale netwerk toonde de volgende resultaten voor sensitiviteit en specificiteit voor de aandoeningen opgenomen in de validatiedataset in 2021:
Tabel 2 – Trends in Sensitiviteit en Specificiteit van het Skinive Neurale Netwerk, 2021–2026
| Nauwkeurigheidsresultaten van het Skinive-neurale netwerk op basis van ziektecategorie | Sensitiviteit, % | Specificiteit, % | ||||||
|---|---|---|---|---|---|---|---|---|
| Pathologiegroep | 2021 | 2022 | 2024 | 2026 | 2021 | 2022 | 2024 | 2026 |
| Goedaardige neoplasmata | 95,0 | 91,7 | 92,5 | 93,1 | 93,0 | 98,2 | 97,9 | 97,4 |
| Acne en rosacea | 88,3 | 96,4 | 96,5 | 97,2 | 99,6 | 99,6 | 99,5 | 99,6 |
| Papulosquameuze aandoeningen | 86,0 | 96,4 | 93,7 | 94,1 | 99,5 | 99,5 | 98,4 | 98,5 |
| Mycosen | 85,5 | 94,7 | 92,1 | 91,7 | 99,8 | 99,9 | 99,3 | 99,3 |
| Virale huidaandoeningen | 82,9 | 88,3 | 87,3 | 87,8 | 99,0 | 98,7 | 98,5 | 99,7 |
| Herpes | 92,6 | 96,0 | 95,1 | 95,7 | 99,7 | 99,9 | 99,7 | 99,7 |
| Precancereuze en maligne neoplasmata | 82,6 | 96,3 | 90,2 | 91,9 | 96,6 | 94,8 | 96,3 | 94,8 |
De resultaten tonen aan dat het Skinive-algoritme consequent een hoge nauwkeurigheid laat zien bij het analyseren van huidafbeeldingen (boven de 90% in de meeste categorieën) en een trend van verbeterde prestaties laat zien tegen 2026.
De grootste vooruitgang in sensitiviteit (het vermogen om tekenen van huidaandoeningen correct te detecteren) werd waargenomen in de categorie “Precancereuze aandoeningen en maligne huidneoplasmata.” De sensitiviteit steeg van 82,6% in 2021 tot 91,9% in 2026. Dit vormt een klinisch significante verbetering, aangezien fouten in deze categorie het meest kritisch zijn. Het algoritme toont ook hoge prestaties in de categorieën “Acne” en “Huidherpes”, met een sensitiviteit van ongeveer 95–97%.
Het handhaven van een hoge specificiteit duidt op een doelbewuste vermindering van fout-positieve resultaten, wat klinisch belangrijk is om onnodige verwijzingen naar medisch specialisten te voorkomen.
De algemene nauwkeurigheidsmetrics van het Skinive-algoritme werden eveneens onderzocht, met de resultaten weergegeven in Tabel 3. Deze metrics karakteriseren de algehele prestaties van het algoritme en de gereedheid om klinische taken uit te voeren.
Tabel 3 – Algemene nauwkeurigheidsmetrics van Skinive van 2021 tot 2026
| Algemene nauwkeurigheidsmetrics van het Skinive-neuraal netwerk | ||||
| Metric, % | 2021 | 2022 | 2024 | 2026 |
| Sensitiviteit | 93,0 | 98,2 | 95,9 | 97,4 |
| Specificiteit | 95,0 | 91,7 | 91,5 | 93,1 |
| Precisie | 80,6 | 72,7 | 75,1 | 82,2 |
| F1-score | 86,4 | 83,5 | 84,2 | 89,1 |
| Nauwkeurigheid | 94,6 | 92,9 | 93,1 | 94,2 |
| Miss Rate | 7,0 | 1,8 | 4,1 | 2,6 |
Vanuit een praktisch perspectief geven deze resultaten aan dat het Skinive-algoritme in de meeste gevallen correct de aanwezigheid van pathologie identificeert, terwijl de kans op valse alarmen ten opzichte van eerdere versies wordt verminderd. Dit is met name belangrijk in het kader van wijdverbreid app-gebruik, waarbij het evenwicht tussen sensitiviteit en specificiteit direct invloed heeft op zowel de veiligheid van de gebruiker als de werkdruk in de gezondheidszorg.
De trend in de algemene nauwkeurigheidsmetrics wordt geïllustreerd in Figuur 4.
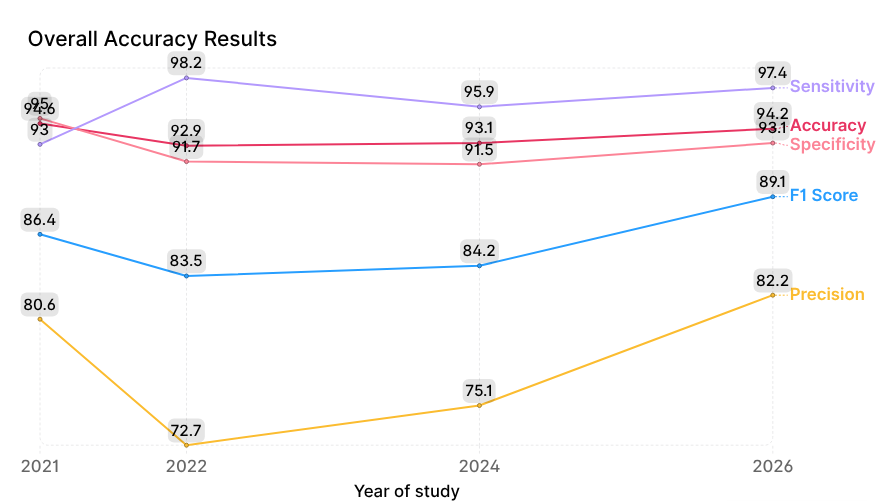
Het belangrijkste aandachtspunt ligt op de dynamiek van twee kernmetrics: sensitiviteit (het minimaliseren van vals-negatieven) en specificiteit (het minimaliseren van vals-positieven). In 2022 piekte de sensitiviteit op 98,2%, maar dit ging ten koste van een lagere specificiteit (91,7%) en precisie (72,7%). Dit weerspiegelt waarschijnlijk een “hyperdiagnose”-effect, waarbij het model voorzichtig te werk ging om te voorkomen dat pathologie werd gemist. Hoewel dit het aantal vals-negatieven vermindert, kan het een onnodige belasting voor de gezondheidszorg veroorzaken door een hoger aantal foutieve verwijzingen.
Latere verbeteringen van het model in 2024 en 2026 leidden tot een lichte daling van de sensitiviteit ten opzichte van 2022, tot 97,4%, terwijl de specificiteit toenam tot 93,1% en de precisie aanzienlijk steeg tot 82,2%.
De stijging van de precisie betekent dat wanneer het algoritme een aandoening als aanwezig aangeeft, dit veel minder vaak onjuist is dan in 2022. Voor gebruikers vertaalt dit zich in minder valse alarmen; voor zorgsystemen vermindert het onnodige bezoeken en werkdruk.
De F1 Score (het harmonisch gemiddelde van precisie en recall) steeg gestaag tot 89,1%, waarmee een maximum werd bereikt. Dit geeft aan dat het model meer gebalanceerd en volwassen is geworden — het “raadt” niet zomaar, maar stelt diagnoses met een optimale afweging tussen type I- en type II-fouten.
De consequent hoge nauwkeurigheid (92–94%) gedurende de gehele observatieperiode toont aan dat het algoritme in het merendeel van de gevallen correct huidcondities kan classificeren. Over het geheel genomen laten deze resultaten zien dat moderne AI-algoritmen huidbeelden met hoge precisie kunnen analyseren en een breed scala aan huidcondities kunnen detecteren, terwijl een balans tussen sensitiviteit en specificiteit wordt gehandhaafd.
Conclusies
De analyse van de prestatie-dynamiek van het Skinive-algoritme van 2021 tot 2026 toont een consistente optimalisatie en verbetering van de kwaliteit van huidbeeldanalyse. Tegen 2026 is het model duidelijk meer in balans: de kloof tussen sensitiviteit en specificiteit wordt kleiner, wat wijst op de “volwassenheid” van het algoritme en een vermindering van zowel vals-negatieve als vals-positieve resultaten. De gepresenteerde resultaten weerspiegelen de prestaties van het algoritme binnen de toegepaste validatiedataset en kunnen variëren afhankelijk van de omstandigheden en kwaliteit van de beeldacquisitie.
In 2022 vertoonde het model een uitgesproken “screening”-gedrag, met maximale sensitiviteit bij matige specificiteit, wat leidde tot een hoog aantal vals-positieve meldingen (precisie 72,7%). Tegen 2026 werd een optimale balans bereikt.
Het handhaven van een nauwkeurigheid van 94,2% en een F1 Score van 89,1%, samen met een gelijktijdige stijging van de precisie tot 82,2%, geeft aan dat het algoritme selectiever en robuuster is geworden bij het analyseren van huidbeelden. Skinive 2026 genereert minder valse meldingen bij het beoordelen van huidveranderingen, terwijl het een hoge capaciteit behoudt om verschillende huidcondities te detecteren. Dit niveau van nauwkeurigheid positioneert het algoritme als een betrouwbaar hulpmiddel voor huidscreening, geschikt voor een eerste evaluatie van huidveranderingen en ter ondersteuning van beslissingen over de noodzaak om een specialist te raadplegen.
Over het geheel genomen laten de resultaten zien dat kunstmatige-intelligentie-algoritmen huidbeelden nauwkeurig kunnen analyseren en tekenen van huidveranderingen kunnen detecteren, terwijl ze een balans tussen sensitiviteit en specificiteit behouden onder realistische omstandigheden.
Om huidcondities te evalueren met AI-technologieën, kunt u de Skinive AI – Huidscanner app gebruiken, ontworpen voor moedervlekanalyse, monitoring van huidveranderingen en het bijhouden van huidgezondheid. Voor het integreren van AI-huidanalyse in uw eigen producten en diensten is de Huidanalyse – API beschikbaar, waarmee huidbeeldanalyse-algoritmen in digitale oplossingen kunnen worden gebruikt.
Auteurs: K. Sokol – Oprichter Skinive B.V., A. Lyan – Hoofd DataScience, V. Shpudeiko – Medisch expert, Oncoloog
Databronnen
- Deng, L.; Li, C.; Li, L.; Mei, Y.; Huang, Q.; Zhang, J. Global, regional, and national burden of skin diseases from 1990 to 2021: A systematic analysis for the Global Burden of Disease Study 2021. International Health 2025, ihaf032. https://doi.org/10.1093/inthealth/ihaf032
- Sung, H.; Ferlay, J.; Siegel, R.L.; Laversanne, M.; Soerjomataram, I.; Jemal, A.; Bray, F. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA: A Cancer Journal for Clinicians 2021, 71, 209–249. https://doi.org/10.3322/caac.21660
- Arnold, M.; Singh, D.; Laversanne, M.; Vignat, J.; Vaccarella, S.; Meheus, F.; Cust, A.E.; de Vries, E.; Whiteman, D.C.; Bray, F. Global Burden of Cutaneous Melanoma in 2020 and Projections to 2040. JAMA Dermatology 2022, 158, 495–503. https://doi.org/10.1001/jamadermatol.2022.0160
- World Health Organization. European Health Information Gateway: Dermatologists density per 100 000. WHO Regional Office for Europe 2015. Доступно онлайн: https://gateway.euro.who.int/
- Chui, M.; Manyika, J.; Miremadi, M. Where machines could replace humans—and where they can’t (yet). McKinsey Quarterly 2016. : https://www.mckinsey.com/
- Maron, R.C.; Haggenmüller, S.; von Kalle, C.; Utikal, J.S.; Meier, F.; Gellrich, F.F.; Hobelsberger, S.; Hauschild, A.; Schlager, J.G.; French, L.; et al. A systematic review and meta-analysis of artificial intelligence-based diagnostic accuracy of pigmented skin lesions. Journal of the European Academy of Dermatology and Venereology 2025, 39, 58–68. https://doi.org/10.1111/jdv.19907
- Li, Q.; Zhang, X.; Zhang, J.; Wang, Y.; Li, Z. Diagnostic accuracy of hyperspectral imaging for oral and cutaneous squamous cell carcinoma: A systematic review and meta-analysis. Oral Diseases 2024, 30, 4224–4235. https://doi.org/10.1111/odi.14985
- Jones, O.T.; Matin, R.N.; van der Schaar, M.; Prathivadi Bhayankaram, K.; Ranmuthu, C.K.I.; Islam, M.S.; Behiyat, D.; Boscott, R.; Calanzani, N.; Emery, J.; et al. Artificial intelligence and machine learning algorithms for early detection of skin cancer in community and primary care settings: a systematic review. The Lancet Digital Health 2023, 5, e466–e480. https://doi.org/10.1016/S2589-7500(23)00093-5
- Smith, A.B.; Johnson, C.D.; Williams, E.F.; Davis, R.K.; Miller, J.L. Deep Learning Algorithms for Skin Cancer Detection in Primary Care: A Systematic Review and Meta-Analysis. Journal of the American Academy of Dermatology 2024, 91, 1124–1133. https://doi.org/10.1016/j.jaad.2024.06.085
- Chen, G.L.; Zhang, L.; Wang, H.; Liu, Y.; Chen, J. Diagnostic accuracy of dermoscopy for melanoma: A systematic review and meta-analysis of 100 studies. British Journal of Dermatology 2024, 190, 523–534. https://doi.org/10.1093/bjd/ljad456
- Lee, I.; Kovarik, C.; Tejasvi, T.; Pizarro, M.; Lipoff, J.B. Teledermatology: A Review and Update. Dermatologic Clinics 2021, 39, 639–649. https://doi.org/10.1016/j.det.2021.05.012
- Zvulunov A, Lenevich S, Migacheva N. A Mobile Health App for Facilitating Disease Management in Children With Atopic Dermatitis: Feasibility and Impact Study. JMIR Dermatol. 2023 Dec 13;6:e49278. doi: https://doi.org/10.2196/49278 . PMID: 38090787; PMCID: PMC10753416.
- Tschandl, P.; Codella, N.; Akay, B.N.; Argenziano, G.; Braun, R.P.; Cabo, H.; Gutman, D.; Halpern, A.; Helba, B.; Hofmann-Wellenhof, R.; et al. Comparison of the accuracy of human readers versus machine-learning algorithms for pigmented skin lesion classification: an open, web-based, international diagnostic study. The Lancet Digital Health 2020, 2, e635–e644. https://doi.org/10.1016/S2589-7500(20)30214-8
- Sokol K, Shpudeiko V. Dynamics of the Neural Network Accuracy in the Context of Modernization of the Algorithms of Skin Pathology Recognition. Indian J Dermatol. 2022 May-Jun;67(3):312. doi: 10.4103/ijd.ijd_1070_21. PMID: 36386072; PMCID: PMC9644746. https://pubmed.ncbi.nlm.nih.gov/36386072/
- Dominique du Crest D, Garibyan L, Hædersdal M, Zink A, Madhumita M, Harth Y, Bechstein S, Friis J, Riemer C, Kumar N, Parkkinen S, Shpudeiko V. Skin & Digital-the 2022 startups. Dermatologie (Heidelb). 2023 Nov;74(11):899-903. English. doi: 10.1007/s00105-023-05204-8. Epub 2023 Aug 8. PMID: 37550513. https://www.researchgate.net/publication/372986021_Skin_Digital-the_2022_startups





