Resumen
Este informe presenta los resultados de un análisis exhaustivo de la precisión del algoritmo de IA Skinive en el análisis de imágenes de la piel desde 2021 hasta 2026. Hoy en día, la inteligencia artificial se utiliza ampliamente en dermatología para el análisis de la piel, la detección de condiciones cutáneas y la identificación de cambios clínicamente relevantes a partir de fotos capturadas con dispositivos móviles.
El algoritmo se evaluó utilizando un conjunto de validación fijo de 27,829 imágenes de piel, lo que permitió una medición consistente y fiable de las mejoras en el rendimiento en las diferentes etapas del desarrollo del modelo. Soluciones como Skinive se emplean cada vez más como herramientas digitales de cribado de la piel, incluidos verificadores de lunares y escáneres de piel con IA que evalúan las condiciones cutáneas a partir de imágenes.
Durante el período de estudio, el algoritmo mostró una mejora constante en los principales indicadores de rendimiento. Para 2026, la sensibilidad alcanzó el 97.4%, la especificidad el 93.1% y la precisión general en el análisis de imágenes de piel llegó al 94.2%. La precisión (precision) aumentó al 82.2%, lo que indica una reducción significativa de los resultados falsos positivos al detectar condiciones cutáneas.
El análisis de las tendencias de rendimiento muestra un claro cambio de un modelo enfocado principalmente en detectar la mayor cantidad posible de anomalías hacia un sistema de IA más equilibrado, capaz de analizar imágenes de piel con precisión mientras minimiza las alertas falsas. Esto es particularmente importante para aplicaciones móviles de escáner de piel y herramientas digitales de dermatología, donde la fiabilidad impacta directamente en la confianza del usuario y en el valor clínico.
El algoritmo se entrenó con más de 3.5 millones de imágenes de piel, de las cuales se seleccionaron 250,000 y fueron validadas por dermatólogos para crear un conjunto de entrenamiento clínicamente fiable. El uso de imágenes reales de usuarios capturadas con smartphones mejora la robustez del modelo frente a variaciones de iluminación, ángulo y calidad de imagen, resultando en un análisis de piel más preciso en condiciones reales.
Estos resultados demuestran que los algoritmos de IA modernos pueden analizar imágenes de piel con alta precisión y detectar signos de condiciones cutáneas, manteniendo un equilibrio sólido entre sensibilidad y especificidad. En dermatología, estas tecnologías se utilizan para evaluar la salud de la piel, analizar lunares, monitorear cambios cutáneos y apoyar la decisión sobre la necesidad de consultar a un dermatólogo.
Por qué la precisión es importante en el análisis de piel con IA
En los últimos años, ha aumentado el interés en cuán precisa puede ser la inteligencia artificial para analizar imágenes de piel y detectar cambios clínicamente relevantes. Esto es especialmente crucial en el contexto de la detección temprana de condiciones de alto riesgo, donde la evaluación oportuna de los cambios en la piel puede desempeñar un papel crítico.
Las enfermedades de la piel siguen siendo un problema de salud global importante. Según el Estudio de la Carga Global de Enfermedad, la prevalencia ajustada por edad de las condiciones cutáneas alcanzó 1,017 casos por cada 100,000 personas en 2021, con una variación regional significativa [1].
El espectro de patologías cutáneas incluye más de 3,000 condiciones distintas. El cáncer de piel tiene especial relevancia:
- El carcinoma basocelular es el cáncer más diagnosticado en todo el mundo.
- El melanoma, aunque menos común, representa la mayoría de las muertes por cáncer de piel [2].
En 2020, hubo 325,000 nuevos casos de melanoma a nivel global, con tasas de supervivencia que oscilaban entre el 50% en Europa del Este y el 80% en Europa Occidental, lo que refleja disparidades en el acceso a cribado, diagnóstico temprano y tratamiento [3].
Este desafío se ve agravado por la escasez continua de especialistas en dermatología. Según la Organización Mundial de la Salud, la disponibilidad de dermatólogos en muchos países europeos sigue siendo insuficiente [4]. En este contexto, las herramientas de análisis de piel basadas en IA son cada vez más importantes como soluciones escalables para cribado y triaje de pacientes [5].
Un creciente cuerpo de investigación respalda la eficacia de la IA en dermatología. Una revisión de 2025 que abarcó 551 estudios encontró que las redes neuronales convolucionales alcanzan el mayor rendimiento diagnóstico, con 91% de sensibilidad y 94% de especificidad al distinguir melanoma de lesiones benignas [6,7].
Es importante destacar que la IA ha demostrado mejorar significativamente la precisión diagnóstica entre médicos generales y profesionales de la salud no especialistas, ofreciendo el mayor beneficio fuera de la dermatología [8].
Un meta-análisis de 2024 evaluando algoritmos de aprendizaje profundo en atención primaria reportó un desempeño sólido, con 90% de sensibilidad y 85% de especificidad en la detección de lesiones pigmentadas sospechosas [9]. La razón de momios diagnóstica alcanzó 26.39 y el área bajo la curva ROC fue 0.95, indicando una excelente capacidad discriminativa.
Estos resultados son comparables a los de dermatólogos experimentados. Según un meta-análisis de 2024 que abarcó 100 estudios, los dermatólogos usando dermatoscopia alcanzaron 85.7% de sensibilidad y 81.3% de especificidad en el diagnóstico de cáncer de piel [10]. Cabe destacar que los dermatólogos experimentados eran 13.3 veces más propensos a realizar diagnósticos precisos comparados con médicos generales.
La pandemia de COVID-19 aceleró la adopción de la teledermatología. Encuestas a profesionales de dermatología mostraron que el uso de telemedicina aumentó del 40% al 90%, con un 87.5% reportando una actitud más positiva hacia la atención remota [11].
La fiabilidad de aplicaciones móviles con IA para el monitoreo remoto de diversas enfermedades dermatológicas, por ejemplo dermatitis atópica, también ha sido confirmada por investigaciones científicas [12].
Los avances en tecnologías de redes neuronales —incluyendo reentrenamiento continuo en conjuntos de datos representativos y mejores estándares de validación— han abordado preocupaciones previas sobre la fiabilidad de soluciones comerciales de IA [13].
Un ejemplo es el algoritmo Skinive AI, que ha mostrado un progreso consistente en el diagnóstico de una amplia gama de condiciones cutáneas y ha sido reconocido por la comunidad científica internacional [14,15]. Este progreso se refleja en la creciente adopción de la app móvil Skinive, que superó 1 millón de descargas en todo el mundo para 2026. La distribución geográfica de los usuarios de Skinive se muestra en la Figura 1.
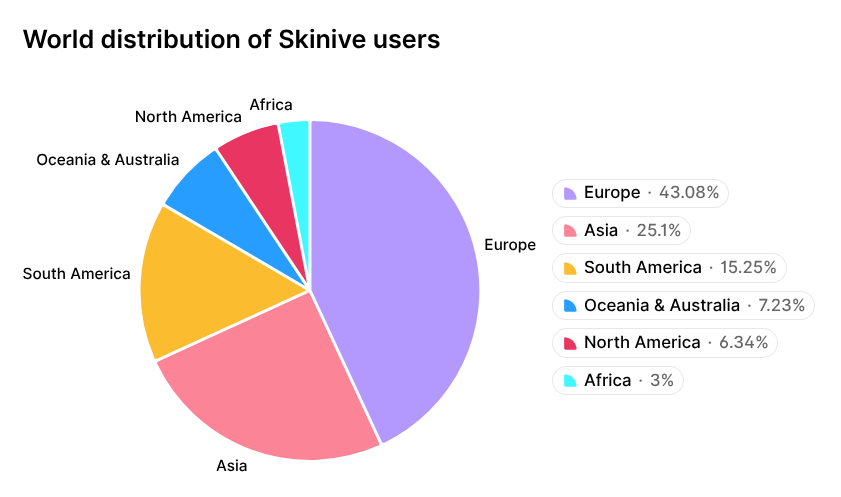
Figura 1. Distribución geográfica de los usuarios de la aplicación móvil Skinive.
Para 2026, las soluciones impulsadas por inteligencia artificial ya no son únicamente herramientas de apoyo: se han integrado cada vez más en los flujos de trabajo de la atención médica, especialmente considerando la escasez continua de especialistas en dermatología y la creciente necesidad de detección temprana de lesiones cutáneas malignas. En consecuencia, la precisión de los algoritmos de IA en dermatología se ha convertido en un factor crítico para su aplicación práctica. La cuestión de cuán confiablemente estos sistemas pueden detectar signos de cambios en la piel es fundamental tanto para los usuarios como para los profesionales de la salud.
Desarrollo del Algoritmo Skinive para el Análisis de Imágenes de la Piel
El avance de los algoritmos de IA impacta directamente en la precisión del análisis de imágenes cutáneas y en la confiabilidad para detectar afecciones de la piel. Esta sección presenta la trayectoria de desarrollo del algoritmo Skinive, destacando mejoras clave en la arquitectura del modelo, la calidad de los datos y la velocidad de procesamiento de imágenes.
La red neuronal Skinive es un sistema de aprendizaje profundo multimodal diseñado para clasificar las características morfológicas de las afecciones cutáneas a partir de imágenes digitales capturadas con cámaras de teléfonos inteligentes. A lo largo de los años, ha experimentado varias mejoras importantes. Las mejoras del algoritmo se centraron en aumentar el tamaño del conjunto de datos, optimizar la arquitectura del modelo y mejorar la calidad del procesamiento de imágenes:
- 2020–2021 (Prototipo): Las primeras versiones se basaron en arquitecturas ResNet y EfficientNet iniciales. El objetivo principal era demostrar la prueba de concepto (PoC) para analizar imágenes de la piel y diferenciar entre condiciones benignas y potencialmente dañinas bajo condiciones de iluminación no controladas.
- 2022–2023 (Validación): El conjunto de datos de entrenamiento creció a más de 160,000 imágenes verificadas. Se introdujo un Módulo de Calidad de Imagen para filtrar imágenes de baja calidad o poco informativas.
- 2024 (Optimización de la Red): La arquitectura de la red neuronal se ajustó mediante optimización de hiperparámetros dirigida.
- 2024–2026 (Escalado y SOTA): Para 2026, Skinive adoptó completamente arquitecturas avanzadas de aprendizaje profundo (Dino v3 Convnext), logrando una alta velocidad de inferencia (360 ms por núcleo). El conjunto de datos final de entrenamiento se amplió a 250,000 imágenes anotadas, etiquetadas por dermatólogos profesionales para garantizar datos de alta calidad y clínicamente validados. La introducción de la arquitectura YOLO11 permitió la detección de objetos en tiempo real en imágenes de piel mediante dispositivos móviles y mejoró aún más la precisión de clasificación.
Estos desarrollos continuos mejoraron significativamente la precisión del análisis cutáneo, aumentaron la capacidad del algoritmo para detectar una amplia gama de afecciones de la piel y redujeron el impacto de factores externos como la calidad de la imagen o la iluminación.
Para alinearse con los estándares clínicos actuales, la clasificación de las afecciones cutáneas reconocidas se actualizó en 2026 y los niveles de riesgo de enfermedad se refinó para reflejar con mayor precisión la relevancia para la salud y la necesidad de consultar a un dermatólogo.
El análisis de las imágenes acumuladas, junto con la retroalimentación de usuarios y socios, indicó la necesidad de entrenar la red neuronal en enfermedades y afecciones cutáneas adicionales. Como resultado, la lista de afecciones reconocibles se amplió para incluir urticaria, eritema, hidradenitis y vitiligo, junto con la capacidad de reconocer uñas saludables (sin patología). La clasificación actual de las afecciones cutáneas reconocidas se presenta en la Tabla 1.
Tabla 1 – Afecciones cutáneas y estados reconocidos por la red neuronal Skinive en 2026
Datos y Conjunto de Entrenamiento de Skinive para el Análisis de Piel Basado en IA
La calidad y el volumen de los datos son factores clave que determinan la precisión de los algoritmos de inteligencia artificial en el análisis dermatológico. Cuanto más diverso y clínicamente validado sea el conjunto de entrenamiento, mayor será la capacidad del algoritmo para analizar correctamente imágenes de la piel en condiciones del mundo real.
Durante un período de seis años, el volumen total de imágenes analizadas por la red neuronal aumentó 300 veces, pasando de 20,000 a 6,000,000 de imágenes, lo que convierte al conjunto de datos de Skinive en una de las bases de datos dinámicamente actualizadas más grandes en dermatología a nivel mundial. La dinámica de crecimiento se ilustra en la Figura 2.
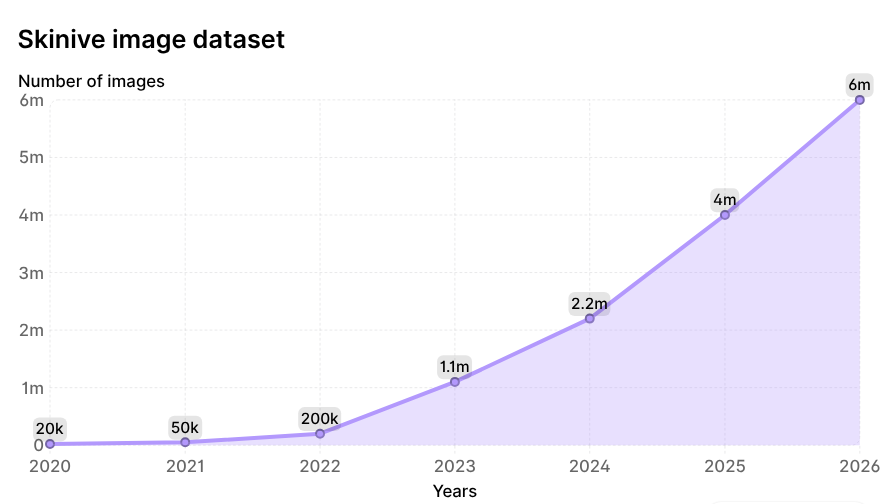
Figura 2. Dinámica de crecimiento de las imágenes analizadas por la red neuronal de Skinive desde 2020.
La distribución geográfica de los usuarios de Skinive, con predominio de las regiones europeas y asiáticas, se refleja de manera natural en la estructura de los fototipos de piel según la escala de Fitzpatrick en el conjunto de datos global (Figura 3). Esta distribución garantiza la representación de diversos fototipos de piel y mejora la robustez del algoritmo al analizar imágenes de distintas poblaciones.
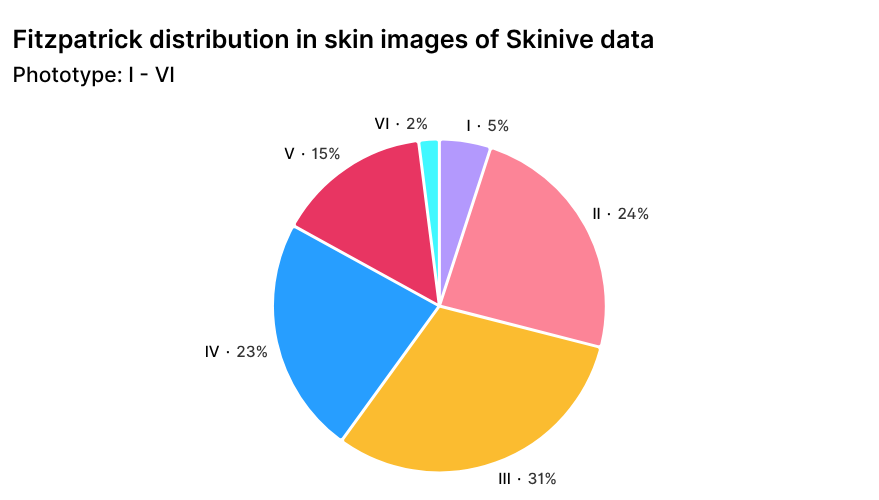
Figura 3. Distribución de las imágenes del conjunto de datos de Skinive según el fototipo de piel, de acuerdo con la escala de Fitzpatrick.
Para formar el conjunto de entrenamiento actual, un panel de expertos dermatólogos analizó 3,5 millones de imágenes. Como resultado de una selección clínica estricta, el conjunto final de entrenamiento incluyó 250,000 imágenes de referencia de alta calidad (tasa de selección ~7%). Esto aseguró un alto grado de validez clínica y consistencia de los datos (“Gold Standard”), crítico para entrenar redes neuronales profundas como Dino v3 Convnext y permite una evaluación objetiva del rendimiento a lo largo del tiempo.
Para evaluar la precisión del algoritmo Skinive, se utilizó un conjunto de validación propietario, creado y estandarizado en 2021. Esto permite una evaluación objetiva del rendimiento del algoritmo en diferentes etapas de desarrollo del modelo. El conjunto de validación comprendía 27,829 imágenes.
La combinación de un conjunto de datos grande, validación clínica y diversidad de condiciones de imagen proporciona una base sólida para mejorar la precisión del análisis de piel basado en IA y hace que el algoritmo sea robusto frente a la variabilidad de las imágenes de usuarios en condiciones reales.
Metodología para Evaluar la Precisión del Algoritmo Skinive
Evaluar la precisión de los algoritmos de IA es un paso crítico en su desarrollo y despliegue. Una metodología de evaluación rigurosa permite determinar cuán confiablemente el algoritmo analiza imágenes de piel y detecta signos de cambios dermatológicos en diversas condiciones.
Este informe presenta un análisis longitudinal interno y estandarizado de la precisión del algoritmo Skinive desde 2021 hasta 2026. El objetivo principal fue evaluar la evolución del rendimiento diagnóstico del modelo a lo largo del tiempo a medida que se sometía a optimizaciones iterativas. A diferencia de estudios comparativos externos, este análisis no se centra en benchmarking frente a otras soluciones, sino en medir el progreso relativo del algoritmo bajo condiciones estrictamente controladas.
Para garantizar la comparabilidad de los resultados a lo largo de todos los años, se utilizó un único conjunto de validación, establecido y fijado en 2021. Este conjunto comprendía 27,829 imágenes que representaban una amplia gama de condiciones dermatológicas, recopiladas bajo condiciones que se aproximan al uso real de dispositivos móviles. El conjunto de validación permaneció sin cambios en los años siguientes y se utilizó exclusivamente para evaluar el rendimiento del modelo, eliminando la variabilidad de los datos como factor confusor y permitiendo comparaciones justas entre diferentes versiones del algoritmo. Es importante destacar que el conjunto de validación nunca se utilizó para entrenar o reentrenar el modelo después de su creación.
La red neuronal se entrenó en un conjunto de datos mucho más grande derivado de la base acumulada de imágenes de usuarios. Inicialmente, se analizaron más de 3,5 millones de imágenes, de las cuales 250,000 se seleccionaron para el conjunto final de entrenamiento. La selección se basó en la relevancia clínica y la calidad de los datos. Solo se incluyeron imágenes que permitieran una interpretación inequívoca de las características morfológicas y contaran con anotaciones verificadas. Se excluyeron imágenes de baja calidad, duplicadas o casos con diagnósticos inciertos o ambiguos. Además, se consideró el balance de clases: cuando el conjunto de datos contenía una sobre-representación de condiciones benignas comunes, se priorizaron enfermedades raras y clínicamente significativas.
Este enfoque para construir el conjunto de entrenamiento aseguró alta integridad de los datos y minimizó el impacto del “ruido” inevitable presente en contenido generado por usuarios. Al mismo tiempo, el conjunto de validación conservó las características del uso en condiciones reales, incluyendo variabilidad en iluminación, calidad de imagen y fototipos de piel, haciendo que la evaluación resultante sea altamente relevante para aplicaciones prácticas, particularmente para imágenes capturadas en dispositivos móviles bajo condiciones diversas.
Se utilizaron métricas de clasificación estándar para evaluar el algoritmo, incluyendo sensibilidad, especificidad, valor predictivo positivo (precisión), F1 Score y exactitud general (accuracy). Todas las métricas se calcularon de manera consistente para cada versión del algoritmo utilizando el mismo conjunto de validación, lo que permitió una evaluación objetiva de los cambios en el rendimiento a lo largo del tiempo. El uso de múltiples métricas proporciona una visión completa de las capacidades del algoritmo, incluyendo su habilidad para detectar condiciones dermatológicas mientras se minimizan los falsos positivos.
Cabe señalar que este análisis se basa en un marco de validación interno y está destinado a evaluar la evolución del algoritmo dentro del ecosistema Skinive. No constituye un estudio clínico externo y no ofrece comparaciones directas con otras soluciones o conjuntos de datos independientes. Se planean estudios comparativos utilizando conjuntos clínicos externos como siguiente etapa en el desarrollo del algoritmo.
Resultados: Precisión del análisis de la piel con Skinive AI
Esta sección presenta los resultados de la evaluación de la precisión del algoritmo Skinive en el análisis de imágenes de la piel. El enfoque se centra en métricas clave como sensibilidad, especificidad y exactitud general (accuracy), que reflejan la capacidad del algoritmo para detectar condiciones dermatológicas mientras se minimizan los falsos positivos.
El análisis de la red neuronal de Skinive mostró los siguientes resultados de sensibilidad y especificidad para las condiciones incluidas en el conjunto de validación en 2021:
Tabla 2 – Tendencias en sensibilidad y especificidad de la red neuronal Skinive, 2021–2026
| Grupo de Patología | Sensibilidad, % | Especificidad, % | ||||||
|---|---|---|---|---|---|---|---|---|
| 2021 | 2022 | 2024 | 2026 | 2021 | 2022 | 2024 | 2026 | |
| Neoplasias benignas | 95.0 | 91.7 | 92.5 | 93.1 | 93.0 | 98.2 | 97.9 | 97.4 |
| Acné y rosácea | 88.3 | 96.4 | 96.5 | 97.2 | 99.6 | 99.6 | 99.5 | 99.6 |
| Trastornos papuloescamosos | 86.0 | 96.4 | 93.7 | 94.1 | 99.5 | 99.5 | 98.4 | 98.5 |
| Micosis | 85.5 | 94.7 | 92.1 | 91.7 | 99.8 | 99.9 | 99.3 | 99.3 |
| Trastornos virales de la piel | 82.9 | 88.3 | 87.3 | 87.8 | 99.0 | 98.7 | 98.5 | 99.7 |
| Herpes | 92.6 | 96.0 | 95.1 | 95.7 | 99.7 | 99.9 | 99.7 | 99.7 |
| Neoplasias precancerosas y malignas | 82.6 | 96.3 | 90.2 | 91.9 | 96.6 | 94.8 | 96.3 | 94.8 |
Los resultados muestran que el algoritmo Skinive demuestra una precisión consistentemente alta en el análisis de imágenes de piel (más del 90 % en la mayoría de las categorías) y presenta una tendencia de mejora del rendimiento hacia 2026.
El mayor progreso en sensibilidad (la capacidad de detectar correctamente los signos de afecciones cutáneas) se observó en la categoría “Condiciones precancerosas y neoplasias cutáneas malignas”. La sensibilidad aumentó del 82,6 % en 2021 al 91,9 % en 2026. Esto representa una mejora clínicamente significativa, ya que los errores en esta categoría son los más críticos. El algoritmo también muestra un alto rendimiento en las categorías “Acné” y “Herpes cutáneo”, con una sensibilidad de alrededor del 95–97 %.
Mantener una alta especificidad indica una reducción deliberada de los falsos positivos, lo cual es clínicamente importante para evitar derivaciones innecesarias a especialistas médicos.
También se examinaron las métricas de precisión general del algoritmo Skinive, cuyos resultados se presentan en la Tabla 3. Estas métricas caracterizan el rendimiento global del algoritmo y su preparación para abordar tareas clínicas.
Tabla 3 – Métricas generales de precisión de Skinive, 2021–2026
| Métricas generales de precisión de la red neuronal Skinive | ||||
| Métrica, % | 2021 | 2022 | 2024 | 2026 |
| Sensibilidad | 93,0 | 98,2 | 95,9 | 97,4 |
| Especificidad | 95,0 | 91,7 | 91,5 | 93,1 |
| Precisión (Valor predictivo positivo) | 80,6 | 72,7 | 75,1 | 82,2 |
| Puntaje F1 | 86,4 | 83,5 | 84,2 | 89,1 |
| Exactitud | 94,6 | 92,9 | 93,1 | 94,2 |
| Tasa de omisión | 7,0 | 1,8 | 4,1 | 2,6 |
Desde un punto de vista práctico, estos resultados indican que el algoritmo Skinive identifica correctamente la presencia de patologías en la mayoría de los casos, al mismo tiempo que reduce la probabilidad de falsas alertas en comparación con versiones anteriores. Esto es especialmente importante en el contexto del uso generalizado de la aplicación, donde el equilibrio entre sensibilidad y especificidad impacta directamente tanto en la seguridad del usuario como en la carga de trabajo de los sistemas de salud.
La tendencia de las métricas generales de precisión se ilustra en la Figura 4.
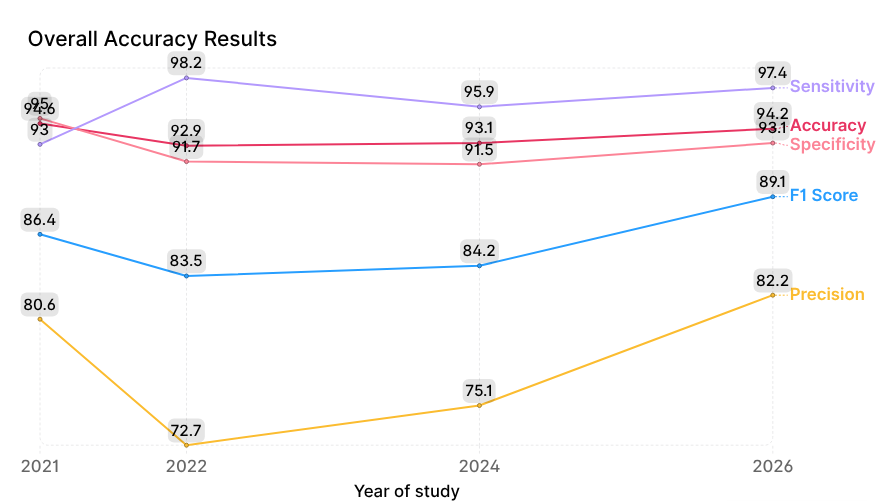
El enfoque principal está en la dinámica de dos métricas clave: sensibilidad (minimización de falsos negativos) y especificidad (minimización de falsos positivos). En 2022, la sensibilidad alcanzó su punto máximo con 98,2 %, pero esto se produjo a costa de una disminución de la especificidad (91,7 %) y de la precisión (72,7 %). Esto probablemente refleja un efecto de “hiperdiagnóstico”, donde el modelo se inclinó por la precaución para evitar pasar por alto cualquier patología. Aunque esto reduce los falsos negativos, puede generar una carga innecesaria en los sistemas de salud debido a un mayor número de derivaciones incorrectas.
Las mejoras posteriores del modelo en 2024 y 2026 resultaron en una ligera reducción de la sensibilidad en comparación con 2022, hasta 97,4 %, mientras que la especificidad aumentó a 93,1 % y la precisión se incrementó significativamente hasta 82,2 %.
El aumento de la precisión significa que, cuando el algoritmo detecta la presencia de una condición, es mucho menos probable que esté equivocado que en 2022. Para los usuarios, esto se traduce en menos falsas alertas; para los sistemas de salud, reduce visitas y cargas innecesarias.
El F1 Score (la media armónica de precisión y recall) aumentó de manera constante hasta 89,1 %, alcanzando su máximo. Esto indica que el modelo se ha vuelto más equilibrado y maduro: no solo “adivina”, sino que realiza diagnósticos con un equilibrio óptimo entre errores tipo I y tipo II.
La alta precisión constante (92–94 %) durante todo el período de observación demuestra la capacidad del algoritmo para clasificar correctamente las condiciones cutáneas en la gran mayoría de los casos. En general, estos resultados muestran que los algoritmos modernos de IA pueden analizar imágenes de piel con gran precisión y detectar una amplia variedad de afecciones cutáneas mientras mantienen un equilibrio entre sensibilidad y especificidad.
Conclusiones
El análisis de la dinámica del rendimiento del algoritmo Skinive de 2021 a 2026 demuestra una optimización constante y una mejora en la calidad del análisis de imágenes cutáneas. Para 2026, el modelo se vuelve claramente más equilibrado: la brecha entre sensibilidad y especificidad se reduce, lo que indica la “maduración” del algoritmo y una disminución tanto de falsos negativos como de falsos positivos. Los resultados presentados reflejan el rendimiento del algoritmo dentro del conjunto de validación aplicado y pueden variar según las condiciones y la calidad de adquisición de las imágenes.
En 2022, el modelo mostró un comportamiento pronunciado de “tamizaje”, alcanzando la máxima sensibilidad con una especificidad moderada, lo que provocó un alto número de alertas falsas (Precisión 72,7 %). Para 2026, se logró un equilibrio óptimo.
Mantener una exactitud (Accuracy) de 94,2 % y un F1 Score de 89,1 %, junto con un aumento simultáneo de la precisión a 82,2 %, indica que el algoritmo se ha vuelto más selectivo y robusto al analizar imágenes de piel. Skinive 2026 genera menos falsas alertas al evaluar cambios cutáneos mientras mantiene una alta capacidad para detectar diversas afecciones. Este nivel de precisión posiciona al algoritmo como una herramienta confiable para el tamizaje de piel, adecuada para la evaluación inicial de cambios cutáneos y para apoyar decisiones sobre la necesidad de consultar a un especialista.
En general, los resultados muestran que los algoritmos de inteligencia artificial pueden analizar imágenes de piel con precisión y detectar signos de cambios cutáneos mientras logran un equilibrio entre sensibilidad y especificidad en condiciones del mundo real.
Para evaluar condiciones de la piel utilizando tecnologías de IA, se puede usar la aplicación Skinive AI – Escáner de Piel, diseñada para análisis de lunares, monitoreo de cambios cutáneos y seguimiento de la salud de la piel. Para integrar capacidades de análisis de piel con IA en sus propios productos y servicios, está disponible el API de Análisis de Piel, que permite utilizar algoritmos de análisis de imágenes de piel en soluciones digitales.
Autores: K. Sokol – Fundador de Skinive B.V., A. Lyan – Jefe de DataScience, V. Shpudeiko – Experto médico, Oncólogo
Fuentes de datos
- Deng, L.; Li, C.; Li, L.; Mei, Y.; Huang, Q.; Zhang, J. Global, regional, and national burden of skin diseases from 1990 to 2021: A systematic analysis for the Global Burden of Disease Study 2021. International Health 2025, ihaf032. https://doi.org/10.1093/inthealth/ihaf032
- Sung, H.; Ferlay, J.; Siegel, R.L.; Laversanne, M.; Soerjomataram, I.; Jemal, A.; Bray, F. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA: A Cancer Journal for Clinicians 2021, 71, 209–249. https://doi.org/10.3322/caac.21660
- Arnold, M.; Singh, D.; Laversanne, M.; Vignat, J.; Vaccarella, S.; Meheus, F.; Cust, A.E.; de Vries, E.; Whiteman, D.C.; Bray, F. Global Burden of Cutaneous Melanoma in 2020 and Projections to 2040. JAMA Dermatology 2022, 158, 495–503. https://doi.org/10.1001/jamadermatol.2022.0160
- World Health Organization. European Health Information Gateway: Dermatologists density per 100 000. WHO Regional Office for Europe 2015. Доступно онлайн: https://gateway.euro.who.int/
- Chui, M.; Manyika, J.; Miremadi, M. Where machines could replace humans—and where they can’t (yet). McKinsey Quarterly 2016. : https://www.mckinsey.com/
- Maron, R.C.; Haggenmüller, S.; von Kalle, C.; Utikal, J.S.; Meier, F.; Gellrich, F.F.; Hobelsberger, S.; Hauschild, A.; Schlager, J.G.; French, L.; et al. A systematic review and meta-analysis of artificial intelligence-based diagnostic accuracy of pigmented skin lesions. Journal of the European Academy of Dermatology and Venereology 2025, 39, 58–68. https://doi.org/10.1111/jdv.19907
- Li, Q.; Zhang, X.; Zhang, J.; Wang, Y.; Li, Z. Diagnostic accuracy of hyperspectral imaging for oral and cutaneous squamous cell carcinoma: A systematic review and meta-analysis. Oral Diseases 2024, 30, 4224–4235. https://doi.org/10.1111/odi.14985
- Jones, O.T.; Matin, R.N.; van der Schaar, M.; Prathivadi Bhayankaram, K.; Ranmuthu, C.K.I.; Islam, M.S.; Behiyat, D.; Boscott, R.; Calanzani, N.; Emery, J.; et al. Artificial intelligence and machine learning algorithms for early detection of skin cancer in community and primary care settings: a systematic review. The Lancet Digital Health 2023, 5, e466–e480. https://doi.org/10.1016/S2589-7500(23)00093-5
- Smith, A.B.; Johnson, C.D.; Williams, E.F.; Davis, R.K.; Miller, J.L. Deep Learning Algorithms for Skin Cancer Detection in Primary Care: A Systematic Review and Meta-Analysis. Journal of the American Academy of Dermatology 2024, 91, 1124–1133. https://doi.org/10.1016/j.jaad.2024.06.085
- Chen, G.L.; Zhang, L.; Wang, H.; Liu, Y.; Chen, J. Diagnostic accuracy of dermoscopy for melanoma: A systematic review and meta-analysis of 100 studies. British Journal of Dermatology 2024, 190, 523–534. https://doi.org/10.1093/bjd/ljad456
- Lee, I.; Kovarik, C.; Tejasvi, T.; Pizarro, M.; Lipoff, J.B. Teledermatology: A Review and Update. Dermatologic Clinics 2021, 39, 639–649. https://doi.org/10.1016/j.det.2021.05.012
- Zvulunov A, Lenevich S, Migacheva N. A Mobile Health App for Facilitating Disease Management in Children With Atopic Dermatitis: Feasibility and Impact Study. JMIR Dermatol. 2023 Dec 13;6:e49278. doi: https://doi.org/10.2196/49278 . PMID: 38090787; PMCID: PMC10753416.
- Tschandl, P.; Codella, N.; Akay, B.N.; Argenziano, G.; Braun, R.P.; Cabo, H.; Gutman, D.; Halpern, A.; Helba, B.; Hofmann-Wellenhof, R.; et al. Comparison of the accuracy of human readers versus machine-learning algorithms for pigmented skin lesion classification: an open, web-based, international diagnostic study. The Lancet Digital Health 2020, 2, e635–e644. https://doi.org/10.1016/S2589-7500(20)30214-8
- Sokol K, Shpudeiko V. Dynamics of the Neural Network Accuracy in the Context of Modernization of the Algorithms of Skin Pathology Recognition. Indian J Dermatol. 2022 May-Jun;67(3):312. doi: 10.4103/ijd.ijd_1070_21. PMID: 36386072; PMCID: PMC9644746. https://pubmed.ncbi.nlm.nih.gov/36386072/
- Dominique du Crest D, Garibyan L, Hædersdal M, Zink A, Madhumita M, Harth Y, Bechstein S, Friis J, Riemer C, Kumar N, Parkkinen S, Shpudeiko V. Skin & Digital-the 2022 startups. Dermatologie (Heidelb). 2023 Nov;74(11):899-903. English. doi: 10.1007/s00105-023-05204-8. Epub 2023 Aug 8. PMID: 37550513. https://www.researchgate.net/publication/372986021_Skin_Digital-the_2022_startups










