Résumé
Ce rapport présente les résultats d’une analyse complète de la précision de l’algorithme Skinive AI pour l’analyse d’images cutanées de 2021 à 2026. Aujourd’hui, l’intelligence artificielle est largement utilisée en dermatologie pour l’analyse de la peau, la détection des affections cutanées et l’identification de modifications cliniquement pertinentes à partir de photos prises avec des appareils mobiles.
L’algorithme a été évalué à l’aide d’un jeu de validation fixe de 27 829 images de peau, permettant une mesure cohérente et fiable des améliorations de performance à différents stades du développement du modèle. Des solutions comme Skinive sont de plus en plus utilisées comme outils de dépistage numérique de la peau, y compris des vérificateurs de grains de beauté et des scanners cutanés alimentés par l’IA qui évaluent les conditions de la peau à partir d’images.
Au cours de la période étudiée, l’algorithme a montré une amélioration régulière des principaux indicateurs de performance. En 2026, la sensibilité a atteint 97,4 %, la spécificité 93,1 %, et la précision globale de l’analyse des images cutanées 94,2 %. La précision (Precision) est passée à 82,2 %, indiquant une réduction significative des résultats faux positifs lors de la détection des affections cutanées.
L’analyse des tendances de performance montre un passage clair d’un modèle principalement axé sur la détection du plus grand nombre possible d’anomalies à un système d’IA plus équilibré, capable d’analyser avec précision les images cutanées tout en minimisant les fausses alertes. Cela est particulièrement important pour les applications mobiles de scanner cutané et les outils de dermatologie numérique, où la fiabilité influence directement la confiance des utilisateurs et la valeur clinique.
L’algorithme a été entraîné sur plus de 3,5 millions d’images de peau, dont 250 000 ont été sélectionnées et validées par des dermatologues afin de créer un jeu de données d’entraînement cliniquement fiable. L’utilisation d’images réelles d’utilisateurs prises sur smartphone améliore la robustesse du modèle face aux variations de lumière, d’angle et de qualité d’image, ce qui permet une analyse cutanée par IA plus précise dans des conditions réelles.
Ces résultats démontrent que les algorithmes d’IA modernes peuvent analyser les images cutanées avec une grande précision et détecter les signes d’affections cutanées tout en maintenant un bon équilibre entre sensibilité et spécificité. En dermatologie, ces technologies sont utilisées pour l’évaluation de la santé de la peau, l’analyse des grains de beauté, le suivi cutané et le soutien à la décision concernant la consultation d’un dermatologue.
Pourquoi la précision est importante dans l’analyse cutanée par IA
Ces dernières années, l’attention portée à la capacité de l’intelligence artificielle à analyser avec précision les images cutanées et à détecter des modifications cliniquement pertinentes s’est accrue. Cela est particulièrement important pour la détection précoce des affections à haut risque, où l’évaluation rapide des changements cutanés peut jouer un rôle crucial.
Les maladies de la peau restent un problème majeur de santé publique mondiale. Selon l’étude Global Burden of Disease, la prévalence standardisée par âge des affections cutanées a atteint 1 017 cas pour 100 000 habitants en 2021, avec des variations régionales significatives [1].
Le spectre des pathologies cutanées comprend plus de 3 000 affections distinctes. Le cancer de la peau revêt une importance particulière :
- Le carcinome basocellulaire est le cancer le plus fréquemment diagnostiqué dans le monde.
- Le mélanome, bien que moins fréquent, est responsable de la majorité des décès liés au cancer de la peau [2].
En 2020, 325 000 nouveaux cas de mélanome ont été recensés dans le monde, avec des taux de survie allant de 50 % en Europe de l’Est à 80 % en Europe de l’Ouest, mettant en évidence les disparités d’accès au dépistage, au diagnostic précoce et au traitement [3].
Ce défi est encore renforcé par la pénurie continue de spécialistes en dermatologie. Selon l’Organisation mondiale de la Santé, la disponibilité des dermatologues dans de nombreux pays européens reste insuffisante [4]. Dans ce contexte, les outils d’analyse cutanée basés sur l’IA deviennent de plus en plus importants comme solutions évolutives pour le dépistage et le tri des patients [5].
Un nombre croissant d’études soutient l’efficacité de l’IA en dermatologie. Une revue de 2025 portant sur 551 études a montré que les réseaux de neurones convolutionnels atteignent la meilleure performance diagnostique, avec une sensibilité de 91 % et une spécificité de 94 % pour différencier le mélanome des lésions cutanées bénignes [6, 7].
Il est important de noter que l’IA améliore significativement la précision diagnostique des médecins généralistes et des prestataires de soins non spécialisés, offrant le plus grand bénéfice en dehors de la dermatologie [8].
Une méta-analyse de 2024 évaluant les algorithmes d’apprentissage profond en soins primaires a rapporté de bonnes performances, avec 90 % de sensibilité et 85 % de spécificité pour la détection des lésions pigmentées suspectes [9]. Le rapport de cotes diagnostique (diagnostic odds ratio) a atteint 26,39 et l’aire sous la courbe ROC 0,95, indiquant une excellente capacité discriminante.
Ces résultats sont comparables à ceux de dermatologues expérimentés. Selon une large méta-analyse de 2024 portant sur 100 études, les dermatologues utilisant la dermoscopie ont atteint 85,7 % de sensibilité et 81,3 % de spécificité dans le diagnostic du cancer de la peau [10]. Il est à noter que les dermatologues expérimentés étaient 13,3 fois plus susceptibles de poser un diagnostic précis par rapport aux médecins généralistes.
La pandémie de COVID-19 a accéléré l’adoption de la télédématologie. Des enquêtes auprès des professionnels de dermatologie ont montré que l’utilisation de la télémédecine est passée de 40 % à 90 %, 87,5 % déclarant une attitude plus positive envers les soins à distance [11].
La fiabilité des applications mobiles utilisant l’intelligence artificielle pour le suivi à distance de diverses maladies dermatologiques, par exemple la dermatite atopique, est également confirmée par la recherche scientifique [12].
Les avancées dans les technologies de réseaux neuronaux — notamment le réentraînement continu sur des ensembles de données représentatifs et l’amélioration des normes de validation — ont permis de résoudre les préoccupations antérieures concernant la fiabilité des solutions d’IA commerciales [13].
Un exemple en est l’algorithme Skinive AI, qui a montré des progrès constants dans le diagnostic d’un large éventail d’affections cutanées et a été reconnu par la communauté scientifique internationale [14, 15]. Ces progrès se reflètent dans l’adoption croissante de l’application mobile Skinive, qui a dépassé 1 million de téléchargements dans le monde en 2026. La répartition géographique des utilisateurs de Skinive est illustrée à la Figure 1.
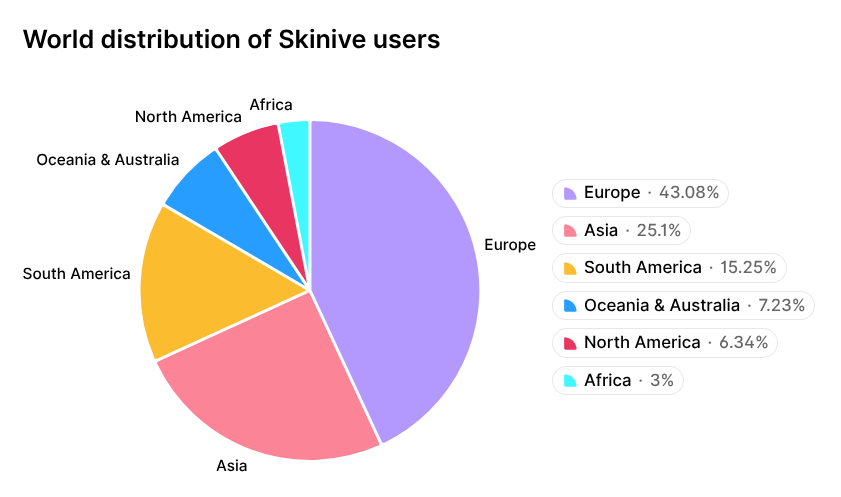
Figure 1. Répartition géographique des utilisateurs de l’application mobile Skinive.
D’ici 2026, les solutions basées sur l’IA ne sont plus de simples outils de soutien : elles sont de plus en plus intégrées aux flux de travail en santé, notamment en raison de la pénurie persistante de spécialistes en dermatologie et du besoin croissant de détection précoce des lésions cutanées malignes. Par conséquent, la précision des algorithmes d’IA en dermatologie est devenue un facteur crucial pour leur utilisation pratique. La question de la fiabilité de ces systèmes pour détecter les signes de changements cutanés est centrale, tant pour les utilisateurs que pour les professionnels de santé.
Développement de l’algorithme Skinive pour l’analyse des images de peau
L’évolution des algorithmes d’IA a un impact direct sur la précision de l’analyse des images cutanées et sur la fiabilité de la détection des affections cutanées. Cette section présente la trajectoire de développement de l’algorithme Skinive, en mettant en évidence les principales améliorations de l’architecture du modèle, de la qualité des données et de la vitesse de traitement des images.
Le réseau neuronal Skinive est un système d’apprentissage profond multimodal conçu pour classifier les caractéristiques morphologiques des affections cutanées à partir d’images numériques capturées avec des caméras de smartphones. Au fil des années, il a subi plusieurs améliorations majeures. Les améliorations de l’algorithme ont porté sur l’augmentation de la taille du jeu de données, l’optimisation de l’architecture du modèle et l’amélioration de la qualité du traitement des images :
- 2020–2021 (Prototypage) : Les premières versions étaient basées sur les architectures ResNet et EfficientNet initiales. L’objectif principal était de démontrer la faisabilité (PoC) pour analyser les images cutanées et différencier les conditions bénignes et potentiellement nocives dans des conditions d’éclairage non contrôlées.
- 2022–2023 (Validation) : Le jeu de données d’entraînement a été porté à plus de 160 000 images vérifiées. Un module de qualité d’image a été introduit pour filtrer les images de faible qualité ou peu informatives.
- 2024 (Optimisation du réseau) : L’architecture du réseau neuronal a été ajustée grâce à une optimisation ciblée des hyperparamètres.
- 2024–2026 (Mise à l’échelle et SOTA) : En 2026, Skinive a adopté pleinement des architectures avancées d’apprentissage profond (Dino v3 Convnext), atteignant une vitesse d’inférence élevée (360 ms par cœur). Le jeu de données d’entraînement final a été élargi à 250 000 images annotées, étiquetées par des dermatologues professionnels pour garantir des données cliniquement validées et de haute qualité. L’introduction de l’architecture YOLO11 a permis la détection d’objets en temps réel sur les images cutanées via des appareils mobiles et a amélioré davantage la précision de classification.
Ces développements continus ont considérablement amélioré la précision de l’analyse cutanée, la capacité de l’algorithme à détecter un large éventail d’affections cutanées, et ont réduit l’impact des facteurs externes tels que la qualité de l’image ou l’éclairage.
Pour s’aligner sur les standards cliniques actuels, la classification des affections cutanées reconnues a été mise à jour en 2026, et les niveaux de risque des maladies ont été affinés pour refléter plus précisément leur pertinence pour la santé et la nécessité de consulter un dermatologue.
L’analyse des images accumulées, ainsi que les retours des utilisateurs et partenaires, a indiqué la nécessité de former le réseau neuronal sur des maladies et conditions cutanées supplémentaires. En conséquence, la liste des conditions reconnaissables a été élargie pour inclure l’urticaire, l’érythème, l’hidradenite et le vitiligo, ainsi que la capacité de reconnaître des ongles sains (sans pathologie). La classification actuelle des affections cutanées reconnues est présentée dans le Tableau 1.
Tableau 1 – Affections cutanées et états reconnus par le réseau neuronal Skinive en 2026
Données et jeu de données d’entraînement de Skinive pour l’analyse cutanée basée sur l’IA
La qualité et le volume des données sont des facteurs clés déterminant la précision des algorithmes d’IA pour l’analyse dermatologique. Plus le jeu de données d’entraînement est diversifié et cliniquement validé, meilleure est la capacité de l’algorithme à analyser correctement les images de peau dans des conditions réelles.
Au cours de cette période de six ans, le volume total d’images analysées par le réseau neuronal a été multiplié par 300, passant de 20 000 à 6 000 000 d’images, faisant du jeu de données Skinive l’une des plus grandes bases de données dermatologiques mises à jour de manière dynamique dans le monde. La dynamique de croissance est illustrée à la Figure 2.
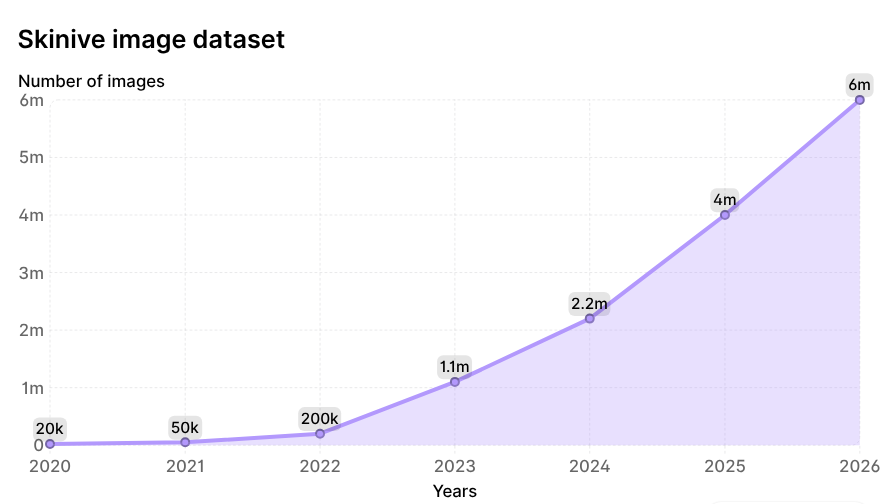
Figure 2. Dynamique de croissance des images analysées par le réseau neuronal Skinive depuis 2020.
La répartition géographique des utilisateurs de Skinive, avec une prédominance des régions européennes et asiatiques, se reflète naturellement dans la structure des phototypes cutanés selon l’échelle de Fitzpatrick dans l’ensemble de données mondial (Figure 3). Cette distribution garantit la représentation de phototypes cutanés diversifiés et renforce la robustesse de l’algorithme lors de l’analyse d’images provenant de différentes populations.
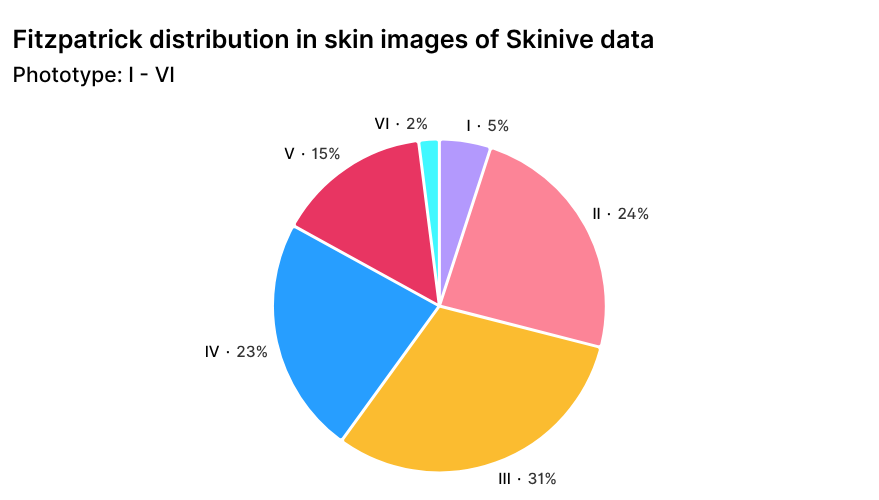
Figure 3. Répartition des images du jeu de données Skinive par phototype cutané selon l’échelle de Fitzpatrick.
Pour constituer l’actuel jeu de données d’entraînement, un panel d’experts dermatologues a analysé 3,5 millions d’images. À la suite d’une sélection clinique stricte, le jeu de données final comprenait 250 000 images de référence de haute qualité (taux de sélection ~7 %). Cela a garanti un haut degré de validité clinique et de cohérence des données (« Gold Standard »), ce qui est crucial pour l’entraînement de réseaux neuronaux profonds tels que Dino v3 Convnext et permet une évaluation objective des performances dans le temps.
Pour évaluer la précision de l’algorithme Skinive, un jeu de données de validation propriétaire a été utilisé, créé et standardisé en 2021. Cela permet une évaluation objective des performances de l’algorithme à différentes étapes du développement du modèle. Le jeu de validation comprenait 27 829 images.
Ainsi, la combinaison d’un grand volume de données, d’une validation clinique et de la diversité des conditions d’imagerie fournit une base solide pour améliorer la précision de l’analyse cutanée basée sur l’IA et rend l’algorithme robuste face à la variabilité des images utilisateur dans des conditions réelles.
Méthodologie d’évaluation de la précision de l’algorithme Skinive
L’évaluation de la précision des algorithmes d’IA est une étape critique de leur développement et de leur déploiement. Une méthodologie rigoureuse permet de déterminer à quel point l’algorithme analyse de manière fiable les images de peau et détecte les signes de modifications dermatologiques dans des conditions variées.
Ce rapport présente une analyse longitudinale interne et standardisée de la précision de l’algorithme Skinive de 2021 à 2026. L’objectif principal était d’évaluer l’évolution des performances diagnostiques du modèle au fil du temps, alors qu’il subissait des optimisations itératives. Contrairement aux études comparatives externes, cette analyse ne vise pas à comparer avec d’autres solutions, mais à mesurer les progrès relatifs de l’algorithme dans des conditions strictement contrôlées.
Pour assurer la comparabilité des résultats sur toutes les années, un seul jeu de données de validation a été utilisé, établi et fixé en 2021. Ce jeu comprenait 27 829 images représentant un large éventail de conditions dermatologiques, collectées dans des conditions proches de l’usage réel sur appareils mobiles. Le jeu de validation est resté inchangé les années suivantes et a été utilisé exclusivement pour évaluer les performances du modèle, éliminant ainsi la variabilité des données comme facteur confondant et permettant des comparaisons équitables entre différentes versions de l’algorithme. Il est important de noter que le jeu de validation n’a jamais été utilisé pour l’entraînement ou le réentraînement du modèle après sa création.
Le réseau neuronal a été entraîné sur un jeu de données beaucoup plus vaste, dérivé de la base d’images accumulées des utilisateurs. Initialement, plus de 3,5 millions d’images ont été analysées, dont 250 000 ont été sélectionnées pour le jeu de données final d’entraînement. La sélection reposait sur la pertinence clinique et la qualité des données. Seules les images permettant une interprétation non ambiguë des caractéristiques morphologiques et dotées d’annotations vérifiées ont été incluses. Les images de faible qualité ou en double, ainsi que les cas présentant un diagnostic incertain ou ambigu, ont été exclus. De plus, l’équilibre des classes a été pris en compte : lorsque le jeu contenait une surreprésentation de conditions bénignes courantes, la priorité a été donnée aux maladies plus rares et cliniquement significatives.
Cette approche de construction du jeu de données d’entraînement a garanti une haute intégrité des données et minimisé l’impact du bruit inévitable présent dans le contenu généré par les utilisateurs. En parallèle, le jeu de validation a conservé les caractéristiques de l’usage réel, y compris la variabilité de l’éclairage, de la qualité des images et des phototypes cutanés, rendant l’évaluation très pertinente pour l’application pratique—en particulier pour les images de peau capturées sur appareils mobiles dans des conditions diverses.
Des métriques de classification standard ont été utilisées pour évaluer l’algorithme, notamment la sensibilité, la spécificité, la valeur prédictive positive (précision), le score F1 et l’exactitude globale. Toutes les métriques ont été calculées de manière cohérente pour chaque version de l’algorithme en utilisant le même jeu de validation, permettant une évaluation objective de l’évolution des performances dans le temps. L’utilisation de multiples métriques fournit une vue complète des capacités de l’algorithme, y compris sa capacité à détecter les conditions dermatologiques tout en minimisant les faux positifs.
Il convient de noter que cette analyse repose sur un cadre de validation interne et vise à évaluer l’évolution de l’algorithme au sein de l’écosystème Skinive. Il ne s’agit pas d’une étude clinique externe et elle ne fournit pas de comparaisons directes avec d’autres solutions ou jeux de données indépendants. Des études comparatives utilisant des jeux de données cliniques externes sont prévues comme prochaine étape du développement de l’algorithme.
Résultats : Précision de l’analyse cutanée par l’IA Skinive
Cette section présente les résultats de l’évaluation de la précision de l’algorithme Skinive dans l’analyse des images de peau. L’accent est mis sur les métriques clés telles que la sensibilité, la spécificité et l’exactitude globale, qui reflètent la capacité de l’algorithme à détecter les conditions dermatologiques tout en minimisant les faux positifs.
L’analyse du réseau neuronal Skinive a montré les résultats de sensibilité et de spécificité suivants pour les conditions incluses dans le jeu de validation en 2021 :
Tableau 2 – Tendances de la sensibilité et de la spécificité du réseau neuronal Skinive, 2021–2026
| Résultats de précision du réseau neuronal Skinive par structure de maladie | Sensibilité, % | Spécificité, % | ||||||
|---|---|---|---|---|---|---|---|---|
| Groupe de pathologies | 2021 | 2022 | 2024 | 2026 | 2021 | 2022 | 2024 | 2026 |
| Tumeurs bénignes | 95,0 | 91,7 | 92,5 | 93,1 | 93,0 | 98,2 | 97,9 | 97,4 |
| Acné et rosacée | 88,3 | 96,4 | 96,5 | 97,2 | 99,6 | 99,6 | 99,5 | 99,6 |
| Affections papulosquameuses | 86,0 | 96,4 | 93,7 | 94,1 | 99,5 | 99,5 | 98,4 | 98,5 |
| Mycoses | 85,5 | 94,7 | 92,1 | 91,7 | 99,8 | 99,9 | 99,3 | 99,3 |
| Affections cutanées virales | 82,9 | 88,3 | 87,3 | 87,8 | 99,0 | 98,7 | 98,5 | 99,7 |
| Herpès | 92,6 | 96,0 | 95,1 | 95,7 | 99,7 | 99,9 | 99,7 | 99,7 |
| Tumeurs précancéreuses et malignes | 82,6 | 96,3 | 90,2 | 91,9 | 96,6 | 94,8 | 96,3 | 94,8 |
Les résultats montrent que l’algorithme Skinive présente une précision globalement élevée dans l’analyse des images cutanées (supérieure à 90 % dans la plupart des catégories) et affiche une tendance à l’amélioration des performances d’ici 2026.
Le plus grand progrès en termes de sensibilité (la capacité à détecter correctement les signes de troubles cutanés) a été observé dans la catégorie « Tumeurs précancéreuses et malignes ». La sensibilité est passée de 82,6 % en 2021 à 91,9 % en 2026. Il s’agit d’une amélioration cliniquement significative, les erreurs dans cette catégorie étant les plus critiques. L’algorithme montre également de bonnes performances dans les catégories « Acné » et « Herpès cutané », avec une sensibilité autour de 95–97 %.
Le maintien d’une spécificité élevée indique une réduction délibérée des résultats faux positifs, ce qui est cliniquement important pour éviter les consultations inutiles chez des spécialistes.
Les métriques globales de précision de l’algorithme Skinive ont également été examinées, avec les résultats présentés dans le Tableau 3. Ces métriques caractérisent la performance générale de l’algorithme et sa capacité à répondre aux tâches cliniques.
Tableau 3 – Métriques globales de précision de Skinive de 2021 à 2026
| Métriques globales de précision du réseau neuronal Skinive | ||||
| Métrique, % | 2021 | 2022 | 2024 | 2026 |
| Sensibilité | 93,0 | 98,2 | 95,9 | 97,4 |
| Spécificité | 95,0 | 91,7 | 91,5 | 93,1 |
| Précision | 80,6 | 72,7 | 75,1 | 82,2 |
| Score F1 | 86,4 | 83,5 | 84,2 | 89,1 |
| Exactitude | 94,6 | 92,9 | 93,1 | 94,2 |
| Taux de manqué | 7,0 | 1,8 | 4,1 | 2,6 |
D’un point de vue pratique, ces résultats indiquent que l’algorithme Skinive identifie correctement la présence de pathologies dans la majorité des cas tout en réduisant la probabilité de fausses alertes par rapport aux versions précédentes. Cela est particulièrement important dans le contexte d’une utilisation étendue de l’application, où l’équilibre entre sensibilité et spécificité impacte directement à la fois la sécurité des utilisateurs et la charge de travail des systèmes de santé.
La tendance des métriques globales de précision est illustrée à la Figure 4.
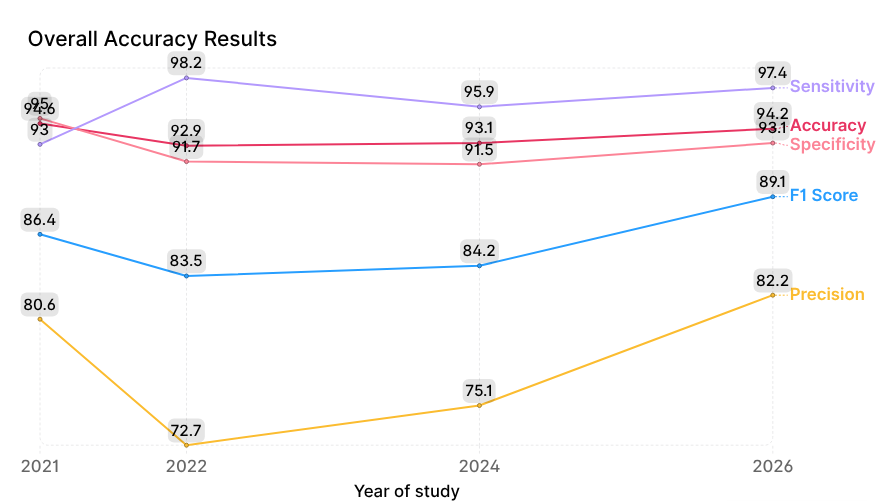
L’accent principal est mis sur la dynamique de deux métriques clés : la sensibilité (minimisation des faux négatifs) et la spécificité (minimisation des faux positifs). En 2022, la sensibilité a atteint un pic de 98,2 %, mais cela s’est fait au prix d’une baisse de la spécificité (91,7 %) et de la précision (72,7 %). Cela reflète probablement un effet de « hyperdiagnostic », où le modèle privilégiait la prudence afin de ne manquer aucune pathologie. Bien que cela réduise les faux négatifs, cela peut créer une charge inutile pour les systèmes de santé en raison d’un plus grand nombre de consultations ou de referrals erronés.
Les améliorations ultérieures du modèle en 2024 et 2026 ont entraîné une légère réduction de la sensibilité par rapport à 2022, à 97,4 %, tandis que la spécificité est passée à 93,1 % et la précision a fortement augmenté pour atteindre 82,2 %.
Cette augmentation de la précision signifie que lorsque l’algorithme signale la présence d’une condition, il est beaucoup moins probable qu’il se trompe qu’en 2022. Pour les utilisateurs, cela se traduit par moins de fausses alertes ; pour les systèmes de santé, cela réduit les visites et la charge de travail inutiles.
Le F1 Score (la moyenne harmonique de la précision et du rappel) a augmenté régulièrement pour atteindre 89,1 %, son maximum. Cela indique que le modèle est devenu plus équilibré et mature : il ne se contente pas de « deviner », mais effectue des diagnostics avec un compromis optimal entre erreurs de type I et type II.
Une précision globalement élevée (92–94 %) sur l’ensemble de la période d’observation démontre la capacité de l’algorithme à classer correctement les affections cutanées dans la grande majorité des cas. Dans l’ensemble, ces résultats montrent que les algorithmes d’IA modernes peuvent analyser les images de la peau avec une grande précision et détecter un large éventail de pathologies tout en maintenant un équilibre entre sensibilité et spécificité.
Conclusions
L’analyse de la dynamique des performances de l’algorithme Skinive de 2021 à 2026 montre une optimisation constante et une amélioration de la qualité de l’analyse des images cutanées. En 2026, le modèle devient clairement plus équilibré : l’écart entre sensibilité et spécificité se réduit, ce qui indique une « maturation » de l’algorithme et une diminution à la fois des faux négatifs et des faux positifs. Les résultats présentés reflètent la performance de l’algorithme sur le jeu de données de validation utilisé et peuvent varier selon les conditions et la qualité des images analysées.
En 2022, le modèle montrait un comportement prononcé de « dépistage », atteignant une sensibilité maximale avec une spécificité modérée, ce qui entraînait un nombre élevé de fausses alertes (Précision 72,7 %). En 2026, un équilibre optimal a été atteint.
Maintenir une précision à 94,2 % et un F1 Score de 89,1 %, avec une augmentation simultanée de la précision à 82,2 %, indique que l’algorithme est devenu plus sélectif et robuste pour l’analyse des images cutanées. Skinive 2026 génère moins de fausses alertes lors de l’évaluation des changements cutanés tout en conservant une grande capacité à détecter diverses pathologies. Ce niveau de précision positionne l’algorithme comme un outil fiable pour le dépistage cutané, adapté à l’évaluation initiale des changements cutanés et au soutien de la décision de consulter un spécialiste.
Dans l’ensemble, les résultats montrent que les algorithmes d’intelligence artificielle peuvent analyser avec précision les images de la peau et détecter les signes de modifications cutanées tout en maintenant un équilibre entre sensibilité et spécificité dans des conditions réelles.
Pour évaluer l’état de la peau à l’aide des technologies d’IA, vous pouvez utiliser l’application Skinive AI – Scanner de Peau, conçue pour l’analyse des grains de beauté, le suivi des changements cutanés et la surveillance de la santé de la peau. Pour intégrer les capacités d’analyse cutanée par IA dans vos propres produits et services, l’API d’Analyse de la Peau est disponible, permettant d’utiliser les algorithmes d’analyse d’images cutanées dans des solutions numériques.
Auteurs : K. Sokol – Fondateur de Skinive B.V., A. Lyan – Responsable DataScience, V. Shpudeiko – Expert médical, Oncologue
Sources des données
- Deng, L.; Li, C.; Li, L.; Mei, Y.; Huang, Q.; Zhang, J. Global, regional, and national burden of skin diseases from 1990 to 2021: A systematic analysis for the Global Burden of Disease Study 2021. International Health 2025, ihaf032. https://doi.org/10.1093/inthealth/ihaf032
- Sung, H.; Ferlay, J.; Siegel, R.L.; Laversanne, M.; Soerjomataram, I.; Jemal, A.; Bray, F. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA: A Cancer Journal for Clinicians 2021, 71, 209–249. https://doi.org/10.3322/caac.21660
- Arnold, M.; Singh, D.; Laversanne, M.; Vignat, J.; Vaccarella, S.; Meheus, F.; Cust, A.E.; de Vries, E.; Whiteman, D.C.; Bray, F. Global Burden of Cutaneous Melanoma in 2020 and Projections to 2040. JAMA Dermatology 2022, 158, 495–503. https://doi.org/10.1001/jamadermatol.2022.0160
- World Health Organization. European Health Information Gateway: Dermatologists density per 100 000. WHO Regional Office for Europe 2015. Доступно онлайн: https://gateway.euro.who.int/
- Chui, M.; Manyika, J.; Miremadi, M. Where machines could replace humans—and where they can’t (yet). McKinsey Quarterly 2016. : https://www.mckinsey.com/
- Maron, R.C.; Haggenmüller, S.; von Kalle, C.; Utikal, J.S.; Meier, F.; Gellrich, F.F.; Hobelsberger, S.; Hauschild, A.; Schlager, J.G.; French, L.; et al. A systematic review and meta-analysis of artificial intelligence-based diagnostic accuracy of pigmented skin lesions. Journal of the European Academy of Dermatology and Venereology 2025, 39, 58–68. https://doi.org/10.1111/jdv.19907
- Li, Q.; Zhang, X.; Zhang, J.; Wang, Y.; Li, Z. Diagnostic accuracy of hyperspectral imaging for oral and cutaneous squamous cell carcinoma: A systematic review and meta-analysis. Oral Diseases 2024, 30, 4224–4235. https://doi.org/10.1111/odi.14985
- Jones, O.T.; Matin, R.N.; van der Schaar, M.; Prathivadi Bhayankaram, K.; Ranmuthu, C.K.I.; Islam, M.S.; Behiyat, D.; Boscott, R.; Calanzani, N.; Emery, J.; et al. Artificial intelligence and machine learning algorithms for early detection of skin cancer in community and primary care settings: a systematic review. The Lancet Digital Health 2023, 5, e466–e480. https://doi.org/10.1016/S2589-7500(23)00093-5
- Smith, A.B.; Johnson, C.D.; Williams, E.F.; Davis, R.K.; Miller, J.L. Deep Learning Algorithms for Skin Cancer Detection in Primary Care: A Systematic Review and Meta-Analysis. Journal of the American Academy of Dermatology 2024, 91, 1124–1133. https://doi.org/10.1016/j.jaad.2024.06.085
- Chen, G.L.; Zhang, L.; Wang, H.; Liu, Y.; Chen, J. Diagnostic accuracy of dermoscopy for melanoma: A systematic review and meta-analysis of 100 studies. British Journal of Dermatology 2024, 190, 523–534. https://doi.org/10.1093/bjd/ljad456
- Lee, I.; Kovarik, C.; Tejasvi, T.; Pizarro, M.; Lipoff, J.B. Teledermatology: A Review and Update. Dermatologic Clinics 2021, 39, 639–649. https://doi.org/10.1016/j.det.2021.05.012
- Zvulunov A, Lenevich S, Migacheva N. A Mobile Health App for Facilitating Disease Management in Children With Atopic Dermatitis: Feasibility and Impact Study. JMIR Dermatol. 2023 Dec 13;6:e49278. doi: https://doi.org/10.2196/49278 . PMID: 38090787; PMCID: PMC10753416.
- Tschandl, P.; Codella, N.; Akay, B.N.; Argenziano, G.; Braun, R.P.; Cabo, H.; Gutman, D.; Halpern, A.; Helba, B.; Hofmann-Wellenhof, R.; et al. Comparison of the accuracy of human readers versus machine-learning algorithms for pigmented skin lesion classification: an open, web-based, international diagnostic study. The Lancet Digital Health 2020, 2, e635–e644. https://doi.org/10.1016/S2589-7500(20)30214-8
- Sokol K, Shpudeiko V. Dynamics of the Neural Network Accuracy in the Context of Modernization of the Algorithms of Skin Pathology Recognition. Indian J Dermatol. 2022 May-Jun;67(3):312. doi: 10.4103/ijd.ijd_1070_21. PMID: 36386072; PMCID: PMC9644746. https://pubmed.ncbi.nlm.nih.gov/36386072/
- Dominique du Crest D, Garibyan L, Hædersdal M, Zink A, Madhumita M, Harth Y, Bechstein S, Friis J, Riemer C, Kumar N, Parkkinen S, Shpudeiko V. Skin & Digital-the 2022 startups. Dermatologie (Heidelb). 2023 Nov;74(11):899-903. English. doi: 10.1007/s00105-023-05204-8. Epub 2023 Aug 8. PMID: 37550513. https://www.researchgate.net/publication/372986021_Skin_Digital-the_2022_startups