概要
本レポートでは、2021年から2026年にかけてのSkinive AIアルゴリズムによる皮膚画像解析精度の包括的な分析結果を示します。現在、人工知能(AI)は皮膚科領域で広く活用されており、皮膚の解析、皮膚疾患の検出、モバイル端末で撮影された画像から臨床的に重要な変化を特定する用途に用いられています。
本アルゴリズムは、27,829枚の皮膚画像で構成された固定検証データセットを使用して評価され、モデル開発の各段階における性能改善を一貫して信頼性高く測定できるようになっています。Skiniveのようなソリューションは、今やデジタル皮膚スクリーニングツールとして、ほくろチェッカーやAI搭載の皮膚スキャナーなど、画像に基づいて皮膚状態を評価するツールとしてますます活用されています。
研究期間を通じて、アルゴリズムは主要な性能指標において着実な改善を示しました。2026年までに感度は97.4%、特異度は93.1%、皮膚画像解析全体の精度は94.2%に達しました。さらに精度(Precision)は82.2%に上昇しており、皮膚疾患の検出時における偽陽性の大幅な削減を示しています。
性能傾向の分析では、異常を可能な限り検出することに重点を置いたモデルから、誤警告を最小限に抑えつつ皮膚画像を正確に解析できる、よりバランスの取れたAIシステムへの明確な移行が確認されました。これは、モバイル皮膚スキャナーアプリやデジタル皮膚科ツールにおいて、信頼性がユーザーの信頼や臨床的価値に直接影響するため、特に重要です。
アルゴリズムは350万枚以上の皮膚画像で学習され、うち25万枚の画像が皮膚科専門医によって選別・検証され、臨床的に信頼性の高い学習データセットが作成されました。スマートフォンで撮影された実際のユーザー画像を使用することで、照明、角度、画像品質の変動に対するモデルの頑健性が向上し、実環境下でのより正確なAI皮膚解析が可能になっています。
これらの結果は、最新のAIアルゴリズムが高精度で皮膚画像を解析し、皮膚疾患の兆候を検出できることを示すとともに、感度と特異度のバランスを維持できることを示しています。皮膚科領域では、このような技術は皮膚の健康評価、ほくろ解析、皮膚のモニタリング、および皮膚科医への相談の必要性判断の意思決定支援に活用されています。
AIによる皮膚解析における精度の重要性
近年、人工知能(AI)が皮膚画像をどれだけ正確に解析し、臨床的に重要な変化を検出できるかに対する関心が高まっています。これは特に、高リスク疾患の早期発見の文脈で重要です。皮膚の変化を迅速に評価することは、患者の予後に大きな影響を与える可能性があります。
皮膚疾患は依然として世界的な重大な健康問題です。世界疾病負担(Global Burden of Disease)研究によると、2021年における皮膚疾患の年齢標準化有病率は人口10万人あたり1,017例であり、地域による差も大きく見られました[1]。
皮膚病理の範囲は3,000以上の異なる疾患を含みます。特に皮膚がんは重要です:
2020年には世界で325,000件の新規メラノーマが報告され、東欧では生存率50%、西欧では80%と地域間の差が存在し、スクリーニング、早期診断、治療へのアクセスの不均衡が浮き彫りになっています[3]。
この課題は、皮膚科専門医の継続的な不足によってさらに悪化しています。世界保健機関(WHO)によると、多くのヨーロッパ諸国では皮膚科医の十分な供給が確保されていません[4]。このような状況下で、AI搭載の皮膚解析ツールは、スクリーニングや患者トリアージのスケーラブルなソリューションとしてますます重要になっています[5]。
AIの皮膚科領域における有効性は、多くの研究によって支持されています。2025年のレビューでは、551件の研究を対象に、畳み込みニューラルネットワーク(CNN)が最高の診断性能を示し、メラノーマと良性皮膚病変を区別する際に感度91%、特異度94%を達成していることが報告されています[6,7]。
重要な点として、AIは一般開業医や非専門医の診断精度を大幅に向上させることが示されており、皮膚科以外の現場で最も大きな効果をもたらします[8]。
2024年の一次診療における深層学習アルゴリズムのメタ分析では、疑わしい色素性病変の検出において感度90%、特異度85%の高い性能が報告されています[9]。診断オッズ比は26.39、ROC曲線下面積(AUC)は0.95であり、優れた識別能力を示しています。
これらの結果は経験豊富な皮膚科医の成績と比較可能です。2024年に実施された100件の研究を対象とする大規模メタ分析によると、皮膚科医がダーモスコピーを使用した場合、皮膚がん診断における感度は85.7%、特異度は81.3%でした[10]。特筆すべきは、経験豊富な皮膚科医は一般開業医に比べて13.3倍正確な診断を行う可能性が高かった点です。
COVID-19パンデミックは、遠隔皮膚科(テレダーモロジー)の採用を加速させました。皮膚科専門家の調査では、遠隔医療の利用率が40%から90%に増加し、87.5%が遠隔診療に対してより前向きな態度を示したことが報告されています[11]。
アトピー性皮膚炎などの様々な皮膚疾患の経過を遠隔でモニタリングするためのAI搭載モバイルアプリの信頼性も、科学的研究によって確認されています[12]。
ニューラルネットワーク技術の進歩—代表的データセットでの継続的再学習や検証基準の改善を含む—により、従来の商用AIソリューションの信頼性に関する懸念は解消されています[13]。
その一例がSkinive AIアルゴリズムであり、幅広い皮膚疾患の診断において一貫した進歩を示しており、世界的な科学コミュニティからも認知されています[14,15]。この進歩は、2026年までに世界で100万ダウンロードを超えたSkiniveモバイルアプリの利用拡大にも反映されています。Skiniveユーザーの地理的分布は図1に示されています。
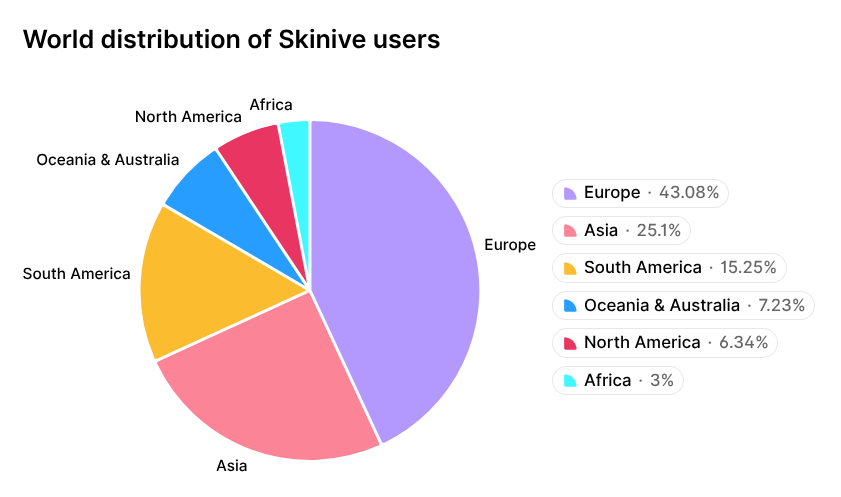
図1. Skiniveモバイルアプリユーザーの地理的分布
2026年までに、AI搭載のソリューションは単なる補助ツールにとどまらず、医療ワークフローにますます統合されるようになりました。特に、皮膚科専門医の継続的な不足や悪性皮膚病変の早期発見の必要性が高まる中で、その重要性は増しています。その結果、皮膚科におけるAIアルゴリズムの精度は、実用面で非常に重要な要素となりました。これらのシステムが皮膚の変化の兆候をどれだけ正確に検出できるかという問題は、ユーザーと医療専門家の双方にとって中心的な関心事です。
皮膚画像解析のためのSkiniveアルゴリズムの開発
AIアルゴリズムの進歩は、皮膚画像解析の精度や皮膚疾患の検出信頼性に直接影響します。本節では、Skiniveアルゴリズムの開発経緯を示し、モデルアーキテクチャ、データ品質、画像処理速度における主要な改善点を強調します。
Skiniveニューラルネットワークは、スマートフォンカメラで撮影されたデジタル画像に基づき、皮膚状態の形態的特徴を分類するために設計されたマルチモーダル深層学習システムです。数年間で、いくつかの大幅な改良が行われました。アルゴリズム改善の主な焦点は、データセットの拡張、モデルアーキテクチャの最適化、および画像処理品質の向上でした。
- 2020–2021(プロトタイピング):初期バージョンはResNetおよび初期のEfficientNetアーキテクチャをベースにしていました。主な目的は、皮膚画像を解析し、制御されていない照明条件下で良性と潜在的に有害な状態を区別する概念実証(PoC)を示すことでした。
- 2022–2023(検証):トレーニングデータセットは16万件以上の検証済み画像に拡張されました。低品質または情報量の少ない画像を除外する「画像品質モジュール」が導入されました。
- 2024(ネットワーク最適化):ニューラルネットワークのアーキテクチャがターゲットを絞ったハイパーパラメータ最適化により微調整されました。
- 2024–2026(スケーリングおよびSOTA):2026年までに、Skiniveは高度な深層学習アーキテクチャ(Dino v3 Convnext)を完全に採用し、高速推論(コアあたり360ms)を達成しました。最終的なトレーニングデータセットは、臨床的に検証された高品質の250,000枚の注釈付き画像に拡張され、専門の皮膚科医によってラベル付けされました。さらに、YOLO11アーキテクチャの導入により、モバイルデバイス上での皮膚画像のリアルタイム物体検出が可能になり、分類精度も向上しました。
これらの継続的な開発により、皮膚解析の精度は大幅に向上し、広範な皮膚状態を検出する能力が高まり、画像品質や照明などの外的要因の影響が軽減されました。
現在の臨床基準に合わせるため、2026年には認識される皮膚状態の分類が更新され、疾患リスクレベルが改良され、健康上の関連性や皮膚科医への相談の必要性をより正確に反映するようになりました。
蓄積された画像とユーザーおよびパートナーからのフィードバックの分析により、ニューラルネットワークを追加の皮膚疾患や状態に対して学習させる必要があることが示されました。その結果、認識可能な状態のリストは、蕁麻疹(じんましん)、紅斑(こうはん)、化膿性汗腺炎(ひだんせんえん)、白斑症(ビチリゴ)に拡張され、さらに健康な爪(病理のない爪)も認識できるようになりました。
認識される皮膚状態の現在の分類は、表1に示されています。
表1 – 2026年にSkiniveニューラルネットワークが認識する皮膚状態と症例
| 10グループ、55の皮膚状態 | |
| 病理グループ | 皮膚状態 |
| 病理なし | 健康な皮膚、健康な爪 ✅ |
| 良性腫瘍 | 良性母斑、乳頭状母斑、手足末端母斑、ハロー母斑、スピッツ母斑、皮膚線維腫、血管腫、化膿性肉芽腫、乳頭腫 🔸、青色母斑 🔸、雀卵斑 🔸、脂漏性角化症 🔸 |
| 前癌状態 | 日光角化症、異形成母斑 |
| 悪性皮膚腫瘍 | 基底細胞がん、扁平上皮がん、メラノーマ、雀卵斑型メラノーマ、角化性棘細胞腫 🔸、ボーエン病 🔸 |
| ウイルス性皮膚疾患 | 尋常性疣贅、扁平疣贅、足底疣贅、伝染性軟属腫 |
| ヘルペス関連皮膚疾患 | 単純ヘルペス、性器ヘルペス、水痘、帯状疱疹 |
| 真菌症 | 皮膚真菌症、爪白癬、毛真菌症、白色癬(花弁状) |
| 紅斑性・鱗屑性疾患 | 尋常性乾癬、膿疱性乾癬、扁平苔癬、紅色苔癬(ピンク苔癬)、光沢苔癬、ドゥヴェルジー苔癬、線状苔癬 |
| ニキビ・酒さ | 尋常性ニキビ、膿疱性ニキビ、嚢胞性ニキビ、閉塞面皰、開放面皰、ミリア、酒さ |
| 皮膚炎、湿疹およびその他の皮膚状態 | アトピー性皮膚炎、皮膚炎、湿疹、脂漏性皮膚炎 🔸、蕁麻疹、紅斑 ✅、化膿性汗腺炎 ✅、白斑症 ✅ |
| ✅ 緑のマーカー — 2026年に追加された状態 🔸 オレンジマーカー — 分類が更新された状態 | |
SkiniveのAIベース皮膚分析のためのデータおよびトレーニングデータセット
データの品質と量は、皮膚科向けAIアルゴリズムの精度を決定する重要な要素です。トレーニングデータセットが多様で臨床的に検証されているほど、アルゴリズムは実際の条件下で皮膚画像を正確に分析する能力が高まります。
6年間の期間で、ニューラルネットワークによって分析された画像の総数は2万枚から600万枚へと300倍に増加し、Skiniveデータセットは世界的に見ても皮膚科分野で最も大規模かつ動的に更新されるデータベースの1つとなりました。成長の動態は図2に示されています。
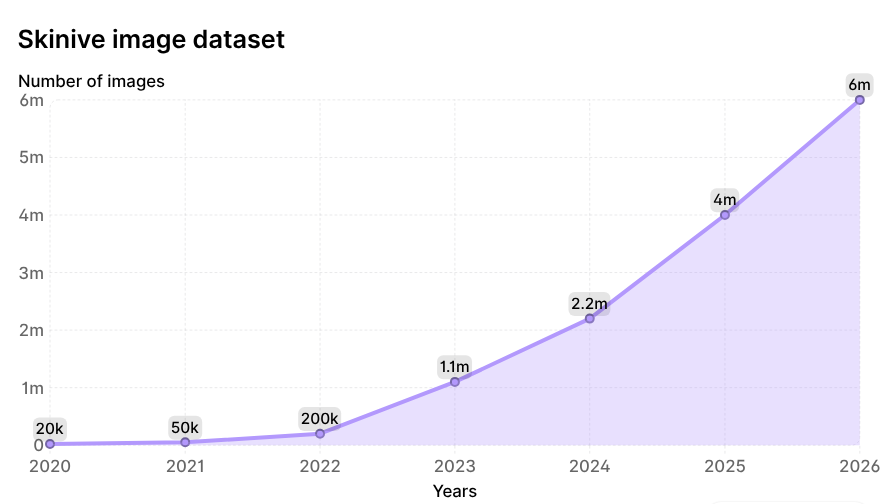
図2. 2020年以降にSkiniveニューラルネットワークで分析された画像の増加動態
Skiniveユーザーの地理的分布は、ヨーロッパおよびアジア地域が中心であり、これは世界的なデータセットにおけるフィッツパトリック・スケールに基づく肌の光タイプ構成にも自然に反映されています(図3)。この分布により、さまざまな肌の光タイプが十分に代表され、異なる人種・地域の画像を解析する際のアルゴリズムの頑健性が向上します。
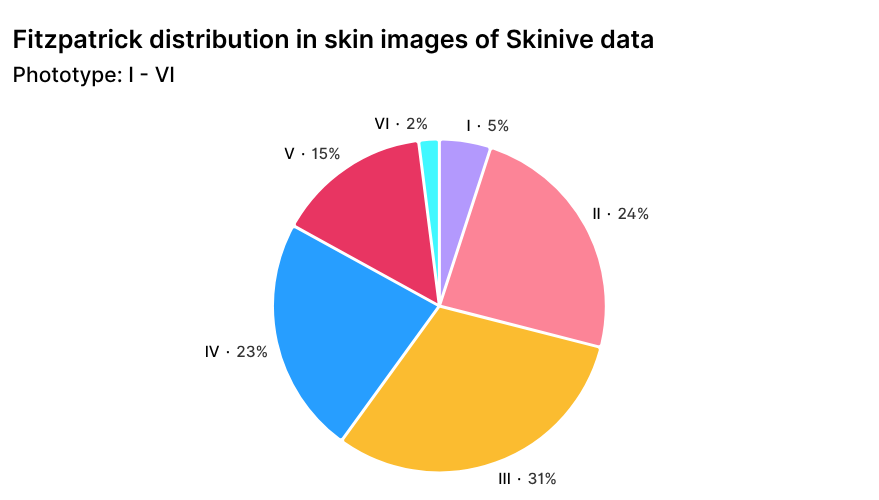
図3. フィッツパトリック・スケールに基づくSkiniveデータセット画像の肌タイプ別分布
現在のトレーニングデータセットを構築するために、皮膚科専門家のパネルが350万枚の画像を分析しました。厳格な臨床選定の結果、最終的なトレーニングデータセットには25万枚の高品質リファレンス画像(選定率:約7%)が含まれました。これにより、臨床的妥当性とデータの一貫性(「ゴールドスタンダード」)が確保され、Dino v3 Convnextのような深層ニューラルネットワークのトレーニングにおいて非常に重要であり、時間を通じた性能評価を客観的に行うことが可能となります。
Skiniveアルゴリズムの精度を評価するために、2021年に作成・標準化された独自の検証データセットが使用されました。これにより、モデル開発の各段階でアルゴリズムの性能を客観的に評価することができます。検証データセットは27,829枚の画像で構成されています。
このように、大規模データセット、臨床的検証、そして多様な撮影条件の組み合わせは、AIによる皮膚分析精度の向上に強力な基盤を提供し、実際のユーザー画像における変動に対してもアルゴリズムの頑健性を高めます。
Skiniveアルゴリズム精度評価の方法論
AIアルゴリズムの精度を評価することは、その開発および導入において重要なステップです。厳密な評価方法により、アルゴリズムが皮膚画像をどれだけ正確に解析し、多様な条件下で皮膚疾患の兆候を検出できるかを判断することが可能になります。
本報告書では、2021年から2026年にかけてのSkiniveアルゴリズムの精度に関する内部標準化縦断分析を示します。主な目的は、反復的な最適化を経たモデルの診断性能の経時的変化を評価することです。外部比較研究とは異なり、本分析は他のソリューションとのベンチマークではなく、厳密に制御された条件下でのアルゴリズムの相対的進歩を測定することに焦点を当てています。
全年度の結果の比較可能性を確保するため、2021年に作成・固定された単一の検証データセットを使用しました。このデータセットは27,829枚の画像で構成され、幅広い皮膚科疾患を代表しており、実際のモバイルデバイス使用状況に近い条件で収集されました。検証データセットはその後の年次でも変更されず、モデル性能の評価のみに使用され、データの変動による混乱要因を排除し、異なるバージョンのアルゴリズム間で公正な比較を可能にしました。重要なのは、この検証データセットは作成後、モデルのトレーニングや再トレーニングには一切使用されていないことです。
ニューラルネットワークは、蓄積されたユーザー画像ベースから派生したはるかに大規模なデータセットでトレーニングされました。最初に350万枚以上の画像が分析され、そのうち25万枚が最終トレーニングデータセットとして選定されました。選定は臨床的重要性とデータ品質に基づいて行われ、形態的特徴の明確な解釈が可能で検証済みの注釈を持つ画像のみが含まれました。低品質または重複画像、診断が不確実または曖昧なケースは除外されました。さらに、クラスバランスも考慮され、一般的な良性疾患が過剰に含まれる場合は、希少で臨床的に重要な疾患に優先順位が付けられました。
このようなトレーニングデータセットの構築手法により、高いデータ整合性が確保され、ユーザー生成コンテンツに必然的に存在するノイズの影響が最小化されます。同時に、検証データセットは照明、画像品質、皮膚タイプの変動など、実際の使用環境の特徴を保持しており、特にモバイルデバイスで撮影された多様な条件下の皮膚画像に対して、実用性の高い評価を可能にしています。
アルゴリズム評価には、感度(sensitivity)、特異度(specificity)、陽性的中率(精度、precision)、F1スコア、および全体精度などの標準分類指標を使用しました。すべての指標は、同一の検証データセットを用いて各アルゴリズムバージョンごとに一貫して計算され、時間経過に伴う性能変化を客観的に評価することが可能です。複数の指標を使用することで、偽陽性を最小化しつつ皮膚疾患を検出する能力など、アルゴリズムの包括的な性能を把握できます。
なお、この分析は内部検証フレームワークに基づくものであり、Skiniveエコシステム内でのアルゴリズムの進化を評価することを目的としています。外部の臨床研究ではなく、他のソリューションや独立したデータセットとの直接比較は行っていません。アルゴリズム開発の次のステップとして、外部臨床データセットを用いた比較研究が計画されています。
結果:Skinive AIによる皮膚画像解析の精度
本章では、Skiniveアルゴリズムによる皮膚画像解析精度の評価結果を示します。重点は、感度(sensitivity)、特異度(specificity)、および全体精度(overall accuracy)などの主要指標に置かれています。これらの指標は、アルゴリズムが皮膚疾患を検出する能力と、偽陽性を最小限に抑える能力を反映しています。
Skiniveニューラルネットワークの解析により、2021年の検証データセットに含まれる疾患に対する感度および特異度の結果は以下の通りでした:
表2 – Skiniveニューラルネットワークの感度および特異度の推移(2021–2026年)
| 疾患構造に基づくSkiniveニューラルネットワークの精度結果 | 感度, % | 特異度, % | ||||||
|---|---|---|---|---|---|---|---|---|
| 病理群 | 2021年 | 2022年 | 2024年 | 2026年 | 2021年 | 2022年 | 2024年 | 2026年 |
| 良性腫瘍 | 95.0 | 91.7 | 92.5 | 93.1 | 93.0 | 98.2 | 97.9 | 97.4 |
| ニキビ・酒さ | 88.3 | 96.4 | 96.5 | 97.2 | 99.6 | 99.6 | 99.5 | 99.6 |
| 紅斑鱗屑性疾患 | 86.0 | 96.4 | 93.7 | 94.1 | 99.5 | 99.5 | 98.4 | 98.5 |
| 真菌症 | 85.5 | 94.7 | 92.1 | 91.7 | 99.8 | 99.9 | 99.3 | 99.3 |
| ウイルス性皮膚疾患 | 82.9 | 88.3 | 87.3 | 87.8 | 99.0 | 98.7 | 98.5 | 99.7 |
| ヘルペス関連疾患 | 92.6 | 96.0 | 95.1 | 95.7 | 99.7 | 99.9 | 99.7 | 99.7 |
| 前癌病変および悪性腫瘍 | 82.6 | 96.3 | 90.2 | 91.9 | 96.6 | 94.8 | 96.3 | 94.8 |
結果は、Skiniveアルゴリズムが皮膚画像の解析において一貫して高い精度(ほとんどのカテゴリーで90%以上)を示しており、2026年までに性能向上の傾向が見られることを示しています。
感度(皮膚疾患の兆候を正確に検出する能力)で最も大きな進歩が見られたのは、「前癌病変および悪性皮膚腫瘍」のカテゴリーでした。感度は2021年の82.6%から2026年には91.9%に向上しました。これは臨床的に重要な改善を示しており、このカテゴリーでの誤診は最も重大です。また、アルゴリズムは「ニキビ」や「皮膚ヘルペス」のカテゴリーでも高い性能を示し、感度は約95〜97%に達しています。
高い特異度を維持することは、偽陽性結果の意図的な削減を意味しており、不要な専門医への紹介を避けるために臨床的に重要です。
Skiniveアルゴリズムの全体的な精度指標も検討され、結果は表3に示されています。これらの指標は、アルゴリズムの総合的な性能と臨床タスクに対応する準備状況を特徴付けます。
表3 – 2021年から2026年までのSkinive全体精度指標
| Skiniveニューラルネットワーク全体の精度指標 | ||||
| 指標, % | 2021年 | 2022年 | 2024年 | 2026年 |
| 感度 | 93.0 | 98.2 | 95.9 | 97.4 |
| 特異度 | 95.0 | 91.7 | 91.5 | 93.1 |
| 精度(Precision) | 80.6 | 72.7 | 75.1 | 82.2 |
| F1スコア | 86.4 | 83.5 | 84.2 | 89.1 |
| 正確度(Accuracy) | 94.6 | 92.9 | 93.1 | 94.2 |
| 見逃し率(Miss Rate) | 7.0 | 1.8 | 4.1 | 2.6 |
実務的な観点から見ると、これらの結果は、Skiniveアルゴリズムがほとんどのケースで病変の存在を正確に特定しつつ、以前のバージョンに比べて誤警告(偽陽性)の可能性を減少させていることを示しています。これは、感度と特異度のバランスがユーザーの安全性や医療システムの負担に直接影響する、広範なアプリ利用の文脈において特に重要です。
全体的な精度指標の推移は、図4に示されています。
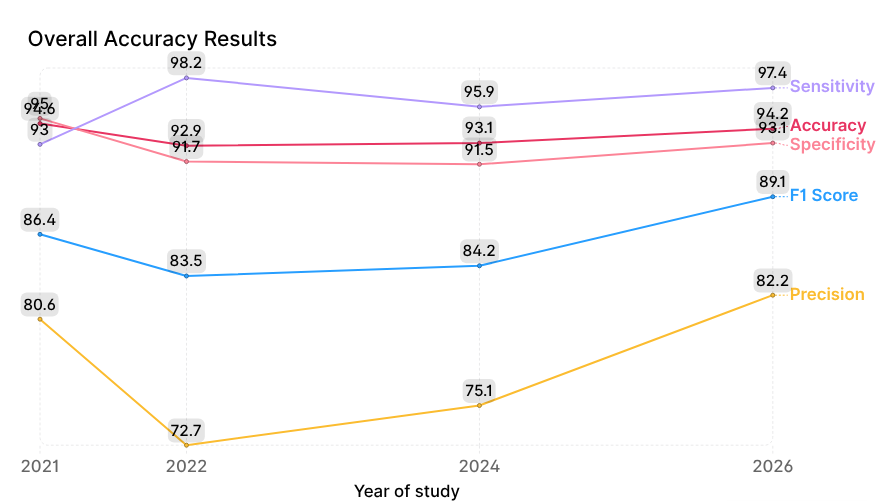
主な焦点は、2つの主要指標の動向にあります:感度(偽陰性を最小化)と特異度(偽陽性を最小化)です。2022年には感度が98.2%でピークに達しましたが、その代償として特異度(91.7%)および精度(72.7%)が低下しました。これはおそらく「過剰診断(ハイパーダイアグノシス)」の効果を反映しており、モデルは病変を見逃さないように慎重に判断した結果です。偽陰性は減少しますが、偽陽性の増加により医療機関への不要な負担が生じる可能性があります。
2024年および2026年のモデル改善により、感度は2022年と比べてわずかに低下し97.4%となった一方、特異度は93.1%に向上し、精度は大幅に82.2%まで上昇しました。
精度の向上は、アルゴリズムが病変を検出した際に誤検出の可能性が2022年よりも大幅に低くなったことを意味します。ユーザーにとっては誤警報が減り、医療機関にとっては不要な受診や業務負荷が軽減されます。
F1スコア(精度と再現率の調和平均)は89.1%まで安定的に上昇し、最大値に達しました。これは、モデルが単なる「推測」ではなく、タイプIおよびタイプIIエラーのバランスを最適化しながら診断を行える、より成熟したバランスの取れた状態であることを示しています。
観察期間全体を通じて92〜94%の一貫した高精度は、アルゴリズムが大多数の症例で皮膚状態を正しく分類できる能力を示しています。全体として、これらの結果は、現代のAIアルゴリズムが高精度で皮膚画像を解析し、幅広い皮膚疾患を検出できる一方で、感度と特異度のバランスも維持できることを示しています。
結論
2021年から2026年にかけてのSkiniveアルゴリズムの性能動向の分析は、皮膚画像解析の品質における一貫した最適化と改善を示しています。2026年までに、モデルは明らかにバランスが向上し、感度と特異度の差が縮小し、偽陰性および偽陽性の両方の減少を示す「成熟」が確認されました。提示された結果は、適用された検証データセット内でのアルゴリズム性能を反映しており、画像取得条件や品質によって変動する可能性があります。
2022年には、モデルは顕著な「スクリーニング」挙動を示し、中程度の特異度で最大感度を達成したため、偽陽性アラートが多く発生しました(精度72.7%)。2026年には、最適なバランスが達成されました。
精度94.2%、F1スコア89.1%を維持し、精度が同時に82.2%に向上したことは、アルゴリズムが皮膚画像解析においてより選択的かつ堅牢になったことを示しています。Skinive 2026は皮膚変化の評価における誤警報を減らしつつ、さまざまな皮膚状態を高精度で検出できる能力を保持しています。この精度レベルは、皮膚スクリーニングの信頼できるツールとして位置付けられ、皮膚変化の初期評価や専門医への受診判断のサポートに適しています。
総じて、結果は人工知能アルゴリズムが現実世界の条件下でも皮膚画像を正確に解析し、皮膚変化の兆候を検出しつつ、感度と特異度のバランスを達成できることを示しています。
AI技術を用いて皮膚状態を評価するには、ほくろ分析、皮膚変化のモニタリング、皮膚健康の追跡を目的とした Skinive AI – Skin Scanner アプリを利用できます。また、独自の製品やサービスにAI皮膚解析機能を統合する場合は、Skin Analysis API を利用することで、皮膚画像解析アルゴリズムをデジタルソリューションに組み込むことが可能です。
著者: K. Sokol – Skinive B.V. 創設者、A. Lyan – データサイエンス責任者、V. Shpudeiko – 医療専門家、腫瘍学者
データソース
- Deng, L.; Li, C.; Li, L.; Mei, Y.; Huang, Q.; Zhang, J. Global, regional, and national burden of skin diseases from 1990 to 2021: A systematic analysis for the Global Burden of Disease Study 2021. International Health 2025, ihaf032. https://doi.org/10.1093/inthealth/ihaf032
- Sung, H.; Ferlay, J.; Siegel, R.L.; Laversanne, M.; Soerjomataram, I.; Jemal, A.; Bray, F. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA: A Cancer Journal for Clinicians 2021, 71, 209–249. https://doi.org/10.3322/caac.21660
- Arnold, M.; Singh, D.; Laversanne, M.; Vignat, J.; Vaccarella, S.; Meheus, F.; Cust, A.E.; de Vries, E.; Whiteman, D.C.; Bray, F. Global Burden of Cutaneous Melanoma in 2020 and Projections to 2040. JAMA Dermatology 2022, 158, 495–503. https://doi.org/10.1001/jamadermatol.2022.0160
- World Health Organization. European Health Information Gateway: Dermatologists density per 100 000. WHO Regional Office for Europe 2015. Доступно онлайн: https://gateway.euro.who.int/
- Chui, M.; Manyika, J.; Miremadi, M. Where machines could replace humans—and where they can’t (yet). McKinsey Quarterly 2016. : https://www.mckinsey.com/
- Maron, R.C.; Haggenmüller, S.; von Kalle, C.; Utikal, J.S.; Meier, F.; Gellrich, F.F.; Hobelsberger, S.; Hauschild, A.; Schlager, J.G.; French, L.; et al. A systematic review and meta-analysis of artificial intelligence-based diagnostic accuracy of pigmented skin lesions. Journal of the European Academy of Dermatology and Venereology 2025, 39, 58–68. https://doi.org/10.1111/jdv.19907
- Li, Q.; Zhang, X.; Zhang, J.; Wang, Y.; Li, Z. Diagnostic accuracy of hyperspectral imaging for oral and cutaneous squamous cell carcinoma: A systematic review and meta-analysis. Oral Diseases 2024, 30, 4224–4235. https://doi.org/10.1111/odi.14985
- Jones, O.T.; Matin, R.N.; van der Schaar, M.; Prathivadi Bhayankaram, K.; Ranmuthu, C.K.I.; Islam, M.S.; Behiyat, D.; Boscott, R.; Calanzani, N.; Emery, J.; et al. Artificial intelligence and machine learning algorithms for early detection of skin cancer in community and primary care settings: a systematic review. The Lancet Digital Health 2023, 5, e466–e480. https://doi.org/10.1016/S2589-7500(23)00093-5
- Smith, A.B.; Johnson, C.D.; Williams, E.F.; Davis, R.K.; Miller, J.L. Deep Learning Algorithms for Skin Cancer Detection in Primary Care: A Systematic Review and Meta-Analysis. Journal of the American Academy of Dermatology 2024, 91, 1124–1133. https://doi.org/10.1016/j.jaad.2024.06.085
- Chen, G.L.; Zhang, L.; Wang, H.; Liu, Y.; Chen, J. Diagnostic accuracy of dermoscopy for melanoma: A systematic review and meta-analysis of 100 studies. British Journal of Dermatology 2024, 190, 523–534. https://doi.org/10.1093/bjd/ljad456
- Lee, I.; Kovarik, C.; Tejasvi, T.; Pizarro, M.; Lipoff, J.B. Teledermatology: A Review and Update. Dermatologic Clinics 2021, 39, 639–649. https://doi.org/10.1016/j.det.2021.05.012
- Zvulunov A, Lenevich S, Migacheva N. A Mobile Health App for Facilitating Disease Management in Children With Atopic Dermatitis: Feasibility and Impact Study. JMIR Dermatol. 2023 Dec 13;6:e49278. doi: https://doi.org/10.2196/49278 . PMID: 38090787; PMCID: PMC10753416.
- Tschandl, P.; Codella, N.; Akay, B.N.; Argenziano, G.; Braun, R.P.; Cabo, H.; Gutman, D.; Halpern, A.; Helba, B.; Hofmann-Wellenhof, R.; et al. Comparison of the accuracy of human readers versus machine-learning algorithms for pigmented skin lesion classification: an open, web-based, international diagnostic study. The Lancet Digital Health 2020, 2, e635–e644. https://doi.org/10.1016/S2589-7500(20)30214-8
- Sokol K, Shpudeiko V. Dynamics of the Neural Network Accuracy in the Context of Modernization of the Algorithms of Skin Pathology Recognition. Indian J Dermatol. 2022 May-Jun;67(3):312. doi: 10.4103/ijd.ijd_1070_21. PMID: 36386072; PMCID: PMC9644746. https://pubmed.ncbi.nlm.nih.gov/36386072/
- Dominique du Crest D, Garibyan L, Hædersdal M, Zink A, Madhumita M, Harth Y, Bechstein S, Friis J, Riemer C, Kumar N, Parkkinen S, Shpudeiko V. Skin & Digital-the 2022 startups. Dermatologie (Heidelb). 2023 Nov;74(11):899-903. English. doi: 10.1007/s00105-023-05204-8. Epub 2023 Aug 8. PMID: 37550513. https://www.researchgate.net/publication/372986021_Skin_Digital-the_2022_startups